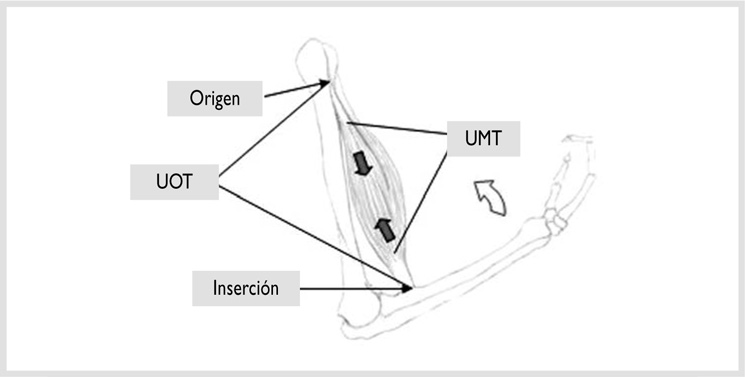
Los tendones son estructuras anatómicas situadas entre el músculo y el hueso cuya función es transmitir la fuerza generada por el primero al segundo, dando lugar al movimiento articular. En la unidad de movimiento básica un músculo tiene dos tendones, uno proximal y otro distal (fig. 1-1). Los tendones y ligamentos poseen tres zonas específicas en toda su longitud: (1) el punto de unión músculo-tendón se denomina unión miotendinosa (UMT); (2) la unión tendón-hueso recibe el nombre de unión osteotendinosa (UOT); (3) en la zona media o cuerpo del tendón éste a veces puede cambiar de dirección apoyándose en las poleas óseas4 24. No siempre ocurre la misma adaptación músculo-tendón; un único tendón, como es el de Aquiles, focaliza la acción de varios músculos o vientres musculares –tríceps sural– con el objetivo de ejercer tracción sobre un solo hueso –calcáneo–, mientras que un solo músculo –tibial posterior– puede actuar sobre varios tendones que, a su vez, anclan en distintas piezas óseas.

FIGURA 1-1. Esquema simplificado de la biomecánica articular. El músculo bíceps braquial se une a sendos tendones en sus exremos (UMT). A su vez, los tendones se insertan en distintos huesos (UOT), para conformar la palanca simple responsable de la movilidad articular. (Abreviaturas, ver texto).
Los tendones presentan un aspecto blanquecino a causa de su relativa avascularidad. Están compuestos de colágeno en un 30% y de elastina en un 2%, todo ello en el seno de una matriz extracelular que contiene hasta un 68% de agua. El colágeno representa alrededor del 70% del peso seco del tendón17 46.
Morfológicamente el tendón varía en forma y tamaño. Puede ser aplanado o redondeado; con respecto al músculo puede encontrarse en el origen, en la inserción o formando intersecciones tendinosas dentro de él. Dentro de un mismo tendón pueden discurrir haces paralelos en un estrato y hacerlo en dirección diferente en estratos adyacentes, siempre en función de la acción muscular, por lo que, en definitiva, lo que determina la configuración del tendón es el estímulo que genera el tipo de movimiento que éste realiza20 50. Además, respecto a los tendones redondeados, el área por sección es proporcional a la fuerza isométrica máxima del músculo al que pertenecen9.
Los tendones pueden estar encapsulados, esto es, rodeados por la membrana sinovial de la articulación; en tal caso se denominan intracapsulares. Los tendones que discurren bajo retináculos se encuentran enclaustrados en túneles fibrosos; ejemplos de ellos son los tendones largos de la mano, la muñeca o el pie.
El grado o amplitud del movimiento de la UMT y la fuerza aplicada al tendón determinan la orientación de las fibras y la mayor amplitud del movimiento del músculo y del tendón11. El tendón, en ocasiones, se halla alejado del músculo al que acompaña, como ocurre en los músculos de los dedos de la mano, cuyos tendones se localizan en el antebrazo.
Los tendones pueden presentar múltiples variaciones en su diseño, de tal modo que pueden ser cortos y gruesos, porque deban transmitir una fuerza importante, como ocurre con el tendón del cuádriceps, o bien largos y finos, como ocurre con los tendones de los dedos, responsables de la ejecución de movimientos delicados, no vigorosos39, o con los tendones peroneos4, que discurren por espacios estrechos.
De acuerdo con la clasificación de Ippolito y Postacchini24, las estructuras que rodean al tendón pueden agruparse en cinco categorías:
1) Las vainas fibrosas son los conductos a través de los cuales los tendones se deslizan durante su recorrido. Están presentes en tendones que tienen que recorrer un largo camino para alcanzar su punto de inserción y pueden, por ello, estar sometidos a importantes fricciones; en ocasiones, los huesos les ofrecen escotaduras y hendiduras provistas de suelo fibrocartilaginoso y cubiertas por una capa fibrosa o retináculo. Ejemplo de ello es el retináculo de los flexores y extensores de la mano y el pie.
2) Las poleas de reflexión son refuerzos anatómicos de las vainas fibrosas localizados en los lugares curvos que se pueden encontrar en el curso del tendón. Su misión en mantener el tendón dentro del lecho por el que se desliza.
3) Las vainas sinoviales son túneles de acceso por los que los tendones acceden al hueso o a otras estructuras anatómicas que pueden causar fricción sobre el tendón. Su finalidad es minimizar dicha fricción. Más frecuentemente se las encuentra alrededor de los tendones de la mano (fig. 1-2) y el pie. Situada bajo una capa fibrosa, la vaina sinovial se compone de dos capas finas y serosas, las vainas parietal y visceral. Estas vainas forman un conducto cerrado que contiene un fluido peritendinoso que se encarga de la lubricación tendinosa.
4) Algunos tendones, como los que carecen de una vaina sinovial verdadera, disponen de una vaina peritendinosa o paratendón para reducir la fricción. Su función es permitir el libre movimiento del tendón contra los tejidos colindantes. Característicamente, el tendón de Aquiles es un claro ejemplo en el que se puede observar el paratendón con finas membranas de deslizamiento. Cuando el paratendón contiene células sinoviales recibe el nombre de tendosinovial; la ausencia de dichas células y la presencia de una doble capa le confiere el nombre de tendovaginal.
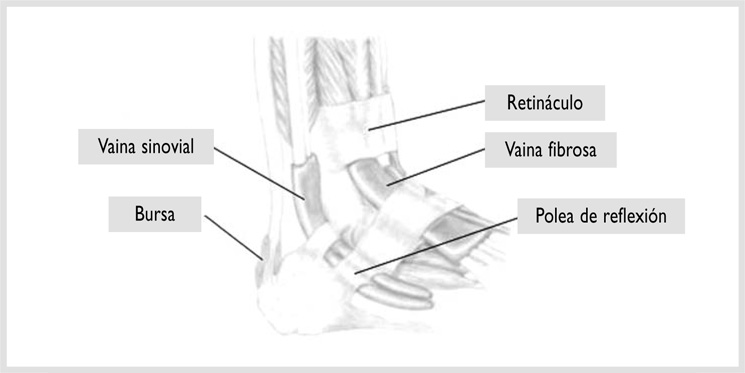
FIGURA 1-2. Elementos extratendinosos en el tobillo: retináculo, vaina fibrosa, vaina sinovial, polea de reflexión, bursa.
5) Las bursas (bolsas) constituyen el quinto tipo de estructura extratendinosa. Son pequeños sacos de líquido situados entre dos estructuras adyacentes –músculo, tendón o hueso– donde actúan como amortiguadores, reduciendo la fricción y asistiendo el movimiento. Juegan un papel importante en la reducción de la fricción. Están localizadas en lugares anatómicamente escogidos donde músculos y tendones pueden sufrir fenómenos compresivos contra prominencias óseas que dificultan el deslizamiento de estas estructuras. Ejemplos de ello son las bursas retrocalcánea, subacromial o infrarrotuliana.
Entre los elementos externos al tendón, son especialmente relevantes las vainas que lo rodean. Las vainas tendinosas se encuentran alrededor del tendón y son comunes en los tendones de la mano y del pie, donde están localizadas en las zonas de largo recorrido curvo –túneles carpiano o del tarso– y en la zona de los dedos. Su principal función es minimizar la fricción entre el tendón y los tejidos que lo rodean22 23.
Las vainas tendinosas tienen dos capas: una externa, que es la vaina fibrosa, y una interna, que es la vaina sinovial; entre ambas existe un espacio virtual que sólo se hace real en situaciones patológicas. La capa externa está compuesta por una red de colágeno cuyas fibras se orientan de manera longitudinal, oblicua o circular respecto al eje del tendón. La superficie interna de la capa fibrosa está tapizada por una capa de células de la cara sinovial parietal, mientras que el tendón está recubierto por las células de la capa visceral. El espacio cerrado –cavidad– entre estas dos capas contiene una fina película de fluido con una composición química similar a la del líquido sinovial articular24.
Existen dos tipos principales de células sinoviales. Las del primer tipo o tipo A son macrófagos y representan el 20-30% de la capa sinovial. Estas células segregan ácido hialurónico, el cual sirve de lubricante para controlar la irritación por fricción y posee, además, función fagocítica26. Las células del segundo tipo o tipo B poseen las características de los fibroblastos y representan el 70-80% del total celular. Estas células también producen líquido sinovial rico en ácido hialurónico. En el citoplasma de estas células encontramos glicoaminoglicanos (GAG) y proteoglicanos (PG) estructurales. Además se puede encontrar una tercera serie de células o tipo C, igualmente de tipo sinovial, forma intermedia entre A y B y que participa en el tejido autoinmune57.
La principal función de la sinovia tendinosa es procurar lubricación, aunque algunos autores han defendido su contribución a la nutrición del tendón15 19 38 40. El mesotendón es característico de los tendones de la mano y pie y tiene dos funciones: primera, anclar el tendón y protegerlo del exceso de rotación, y segunda, proporcionar la placa por la que vasos y nervios penetran en el tejido del tendón46.
El tendón está constituido por distintos elementos: células, sustancia fundamental y fibras de colágeno (tabla 1-1), todo ello mantenido por diferentes tipos de enlace. Estos elementos constituyen el cuerpo del tendón en distintas proporciones26:
TABLA 1-1. Componentes del tendón.
Células | Fibroblasto es la célula predominante |
Sustancia fundamental |
Elementos más frecuentes: proteoglicanos y agua |
Fibras de colágeno |
Moléculas de colágeno empaquetadas como miofibrillas |
Son numerosos los tipos de células que se encuentran en la sustancia fundamental del tejido conectivo. Algunas son fijas, es decir, pertenecen a una población permanente, mientras que otras van y vienen de forma aleatoria respondiendo a las necesidades del tejido.
(i) Los fibroblastos son las células constantes del tejido conectivo. Adoptan diversos aspectos morfológicos, aunque la mayor parte de ellos tienen forma de huso. Muy numerosos, son los responsables de la formación de los componentes fibrosos del tejido conectivo, el colágeno y la elastina. De igual modo, están implicados en la elaboración de la sustancia fundamental amorfa y de mediadores celulares del proceso de curación. De ahí que presenten cierta movilidad en respuesta al traumatismo y la inflamación. No en vano la proliferación fibroblástica tiene un papel crucial en el proceso de reparación tendinoso35. Carecen de regulación central, por lo que las modificaciones de su forma, función y composición obedecen a estímulos locales, principalmente de carácter mecánico20.
(ii) Los macrófagos son particularmente numerosos en el tejido conectivo laxo. Se mueven libremente y juegan un papel en el sistema reticuloendotelial. Son carroñeros activos, engullendo células muertas, bacterias y partículas extrañas. También liberan muchos de los mediadores que generan la respuesta inflamatoria24.
(iii) Las células cebadas se encuentran cerca de los vasos sanguíneos y su función es muy controvertida. Producen anticoagulantes como la heparina, aunque también liberan histamina y serotonina. Estas sustancias vasoactivas, conocidas como cininas, participan en el control del flujo de sangre a la zona, especialmente en el proceso inflamatorio.
Aunque sea sólo en determinadas circunstancias, cabe encontrar otras células como linfocitos y neutrófilos polimorfonucleares, que intervienen en el sistema de defensa celular y humoral24.
La llave de la fuerza del tejido conectivo es la configuración de la molécula de colágeno. El colágeno comprende una familia de moléculas divididas en dos grupos mayores. Se identifican 13 tipos de colágeno (tabla 1-2), los cuales pueden ser divididos en dos clases: los que conforman fibras regulares de colágeno (I, II, III, V, XI) y los que no las conforman (IV, VI, VII, VIII, IX, XII, XIII). Los tipos II y IX se encuentran únicamente en el cartílago. El colágeno presente en el tendón es en su mayoría de tipo I, constituyendo el 70-80% del peso seco del tendón. Los demás tipos se encuentran en cantidades menores. Entre todos ellos configuran las propiedades mecánicas del tendón13 32.
TABLA 1-2. Características de los diferentes tipos de colágeno. Adaptado de: Eyre DR. The collagens of musculoskeletal soft tissue. En: Leadbetter WB, Buckwater JA, Gordon SI. Sports-induced inflammation. Park Ridge:AAOS; 1990.
Tipo |
Tejido |
Forma |
Tipo I |
Hueso, piel,tendón |
Fibrilar |
Tipo II |
Cartílago, disco |
Fibrilar |
Tipo III |
Piel, tendón, vasos sanguíneos |
Fibrilar |
Tipo IV |
Lámina basal |
Red tridimensional |
Tipo V |
Con tipo I |
Fibrilar |
Tipo VI |
Extendido |
Microfilamentos |
Tipo VII |
Membrana epitelial |
Inserción fibrilar |
Tipo VIII |
Membrana endotelial |
Desconocida |
Tipo IX |
Cartílago |
Enlace cruzado |
Tipo X |
Cartílago hipertrófico |
Desconocida |
Tipo XI |
Con tipo I |
Fibrilar |
Tipo XII |
Tendón, ¿otros? |
Desconocida |
Tipo XIII |
Células endoteliales |
Desconocida |
Es una sustancia amorfa en cuyo seno ocurren la configuración y deambulación de las distintas fibras y células. La sustancia fundamental o matriz extracelular contribuye de manera importante a la integridad mecánica del tendón, al desarrollo de los tejidos, a su organización y al control de su crecimiento44. Su composición responde a una mezcla de agua, PG y GAG. La sustancia fundamental aporta el cemento que causa que las fibras de colágeno se adhieran unas a otras y proporcionen lubricación y espacio para que puedan deslizarse unas sobre otras.
Los GAG representan sólo el 1% del peso seco del tendón, pero su importancia radica en su capacidad para retener agua, la cual constituye el 65-75% del peso total del tendón. Los GAG son biomoléculas de azúcar que pueden combinarse con otros GAG para formar cadenas largas, o con proteínas, para formar glicoproteínas del tipo fibronectina, tenascina o fibromedulina, fundamentales en la regulación y establización de la matriz extracelular11 32 46.
No todos los tendones poseen una composición uniforme en toda su longitud, sino que tienen variaciones locales en cuanto al contenido de agua, GAG y colágeno para ajustarse a las particularidades biomecánicas en su recorrido. Cuando los tendones discurren por las poleas óseas tienen un contenido preferente de colágeno tipo II3 y su contenido en GAG es muy alto4.
Las moléculas de tropocolágeno están estabilizadas y se mantienen unidas mediante enlaces electrostáticos y químicos denominados enlaces cruzados. Si la sustancia fundamental aporta el espacio físico, la estabilidad molecular la aportan los enlaces cruzados. Estas moléculas se encuentran unidas mediante enlaces covalentes tanto a nivel intramolecular –cadenas α?del mismo tropocolágeno–, como intermolecular –entre moléculas adyacentes de tropocolágeno–7 14.
Diferentes cadenas de aminoácidos son conectadas mediante enlaces intermoleculares para formar fibrillas que darán lugar a la fibra. Los enlaces cruzados son importantes para la fuerza tensil del colágeno, haciéndolo más fuerte por unidad y con capacidad para absorber más energía, lo que aumenta su resistencia al ser sometido a tensión.
Las sustancias químicas de los enlaces se producen durante el metabolismo normal y son renovadas por procesos metabólicos durante la primera etapa de la vida, pero se acumulan en los individuos mayores26 42. De ahí que los tendones en la edad avanzada sean más rígidos y menos elásticos.
Hasta comienzos del siglo XX el tendón fue considerado un elemento avascular y metabólicamente inactivo. Es en 1916 cuando se demuestra el aporte vascular al tendón a través de la inyección con colorantes, admitiéndose entonces que el tendón recibe cierto aporte sanguíneo procedente del mesotendón41. A partir de los trabajos de Smith, en 1965, se atribuye al tendón una actividad metabólica propiciada por su flujo continuo de sangre49.
El aporte sanguíneo al tendón proviene en su mayoría del músculo. El abordaje vaso-tendón difiere en función del segmento tendinoso, considerando el tendón en tres regiones: UMT, cuerpo del tendón y UOT. Los vasos sanguíneos se originan desde microvasos en el perimisio8.
En la UMT los vasos sanguíneos del perimisio muscular continúan entre los fascículos del tendón y son del mismo tamaño que los vasos en el músculo24 48 (fig. 1-3).
En la porción media del tendón el aporte vascular llega vía paratendón o a través de la vaina sinovial34. Son vasos de menor tamaño, por lo que esta zona está peor perfundida, lo que la convierte en una zona crítica lesional37. Los tendones que están expuestos a la fricción y están encerrados en una vaina sinovial reciben el aporte sanguíneo a través de la membrana sinovial. Si no existe membrana sinovial, la perfusión sanguínea ocurre a partir de la red vascular del paratendón. Los pequeños vasos del paratendón discurren transversalmente hacia el tendón, mientras que otras ramas lo hacen paralelas al eje del tendón. Los vasos penetran el epitendón y recorren el endotendón para formar la red vascular intratendinosa (fig. 1-3). Las arteriolas discurren longitudinalmente flanqueadas por dos vénulas23 24.
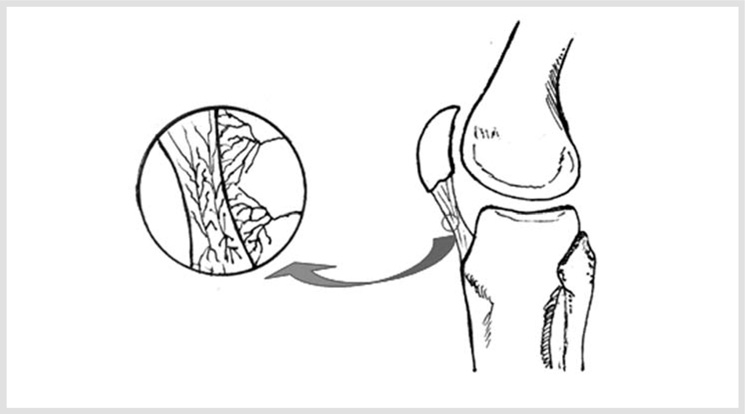
FIGURA 1-3. Aporte vascular al tendón rotuliano. Se observa cómo una fina red vascular invade las capas más externas del tendón procedentes de la grasa amarilla; por otro lado, se observa la disposición vascular en paralelo al paratendón.
Los vasos que irrigan la UOT suministran el tercio externo del tendón. No están comunicados directamente los vasos procedentes del hueso con los que proceden del tendón, debido a la presencia de una membrana fibrocartilaginosa entre el tendón y el hueso, pero existe alguna anastomosis indirecta entre estos vasos. De cualquier modo, su aporte sanguíneo es menor y no contribuye a la vascularización del cuerpo del tendón22 29 37.
La configuración espacial de la red vascular depende de la morfología del tendón; es larga y uniforme para tendones como el rotuliano o el de Aquiles, y ancha y estrellada para los tendones flexores de los dedos.
El aporte sanguíneo al tendón aumenta durante el ejercicio y ante los procesos de curación2 6, y se ve disminuido cuando es sometido a tensión o en determinadas zonas de fricción, torsión o compresión. Existen diferentes lugares en el organismo anatómicamente predispuestos al deterioro vascular. Quizá el lugar donde esta circunstancia es más evidente lo constituye el tendón del supraespinoso22 46, en el que las posiciones de aproximación o elevación del húmero en el plano sagital agravan el déficit sanguíneo48. En el tendón de Aquiles ha sido también identificada una zona de relativa avascularidad16 24 48, así como en la cara dorsal del flexor profundo de los dedos, en el primer centímetro previo a la inserción36.
Por lo general, la vascularidad del tendón es más deficitaria en los hombres que en las mujeres y disminuye con la edad y la sobrecarga mecánica1. Durante el ejercicio el aporte sanguíneo aumenta, independientemente de la edad, si bien alrededor del tendón sólo alcanza el 20% de la capacidad máxima en comparación con lo que puede conseguir durante la hiperemia reactiva5.
La inervación del tendón es esencialmente aferente. Los nervios acceden al tendón cerca de la UMT y forman pequeños plexos longitudinales, los cuales, desde la UMT, atraviesan ésta y penetran en el septo del endotendón. Desde el paratendón forman ricos plexos que envían ramos que penetran en el epitendón y se anastomosan con los ramos de origen muscular (fig. 1-4). Si el tendón está provisto de vaina sinovial, los nervios atraviesan el mesotendón y dan ramas hacia la pared visceral de la membrana sinovial, penetrando desde ella en el tendón. Dentro del tendón el nervio se desliza a lo largo de su eje y finaliza en terminaciones nerviosas sensoriales24 26.
De acuerdo con los criterios funcionales y anatómicos, las terminaciones nerviosas en los tendones se pueden clasificar en cuatro categorías18 24 25 27: tipo I o corpúsculos de Ruffini, que son receptores de presión y reaccionan lentamente a los cambios de presión; tipo II o corpúsculos de Paccini, que también reaccionan a la presión pero son de adaptación rápida, ya que intervienen en la detección de movimientos de aceleración y desaceleración; tipo III o terminaciones de Golgi, las cuales son mecanorreceptores cuya función es convertir la deformación mecánica, expresada en presión o tensión –contracción o elongación musculares–, en señales nerviosas aferentes. La tensión muscular se transmite al tendón e induce la compresión de las terminaciones nerviosas por medio de las fibras de colágeno, generando potenciales axonales que sinaptan con las neuronas de interconexión de la médula espinal e inhiben las neuromotoras α. Todos ellos tienen un importante papel en la organización del sistema sensorial neuronal aferente que controla los movimientos del cuerpo vía sistema nervioso central. El tipo IV son las terminaciones nerviosas libres, que son receptores del dolor de adaptación lenta.
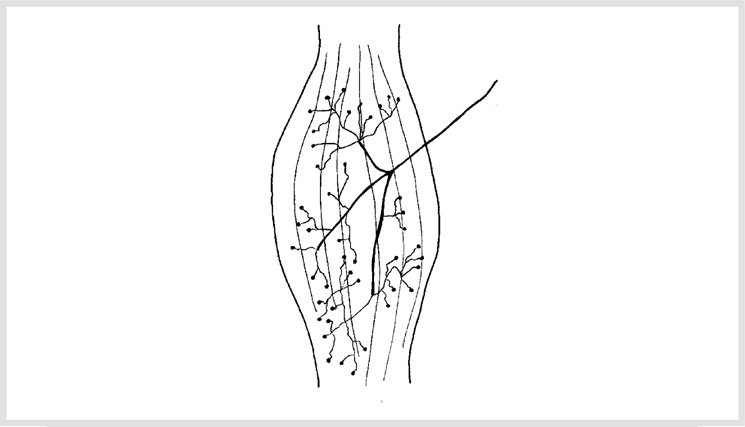
FIGURA 1-4. Acceso neuronal al cuerpo del tendón. En este caso se muestra la distribución de las terminaciones de Golgi.
Los tendones inmersos en movimientos sofisticados –por ejemplo, flexores de los dedos– poseen una inervación superior a la de otros tendones comprometidos en movimientos más primarios –como el tendón de Aquiles–59. Por otro lado, la inervación es mayor cerca de la UMT que de la UOT25 27.
La síntesis de colágeno comprende dos procesos que tienen lugar tanto en el interior como en el exterior de la célula.
El colágeno posee como unidad estructural al tropocolágeno. El tropocolágeno es la unidad mínima, una única proteína larga y delgada formada por colágeno de tipo I. El entrecruzamiento de tres secuencias de aminoácidos en triple hélice da lugar a una molécula de procolágeno. De estas secuencias o cadenas polipeptídicas, dos poseen una estructura primaria y reciben el nombre de cadena α-1, en tanto que la tercera tiene una composición de aminoácidos diversos y se denomina cadena α-251 (fig. 1-5).
Las cadenas de aminoácidos se conectan mediante puentes intermoleculares, mientras que las moléculas de tropocolágeno se encuentran unidas por medio de enlaces electrostáticos.
La principal característica del proceso intracelular es la hidroxilación y glicolización de los aminoácidos, la formación de cadenas terciarias y la unión por medio de enlaces covalentes. La presencia de las cadenas largas polipeptídicas dota de estabilidad y calidad a la fibra de colágeno47. Estas cadenas de aminoácidos se entrecruzan en formaciones terciarias unidas por enlaces covalentes, formando una cadena en triple hélice que recibe el nombre de procolágeno (fig. 1-6). La molécula de procolágeno es entonces secretada al espacio extracelular mediante exocitosis.
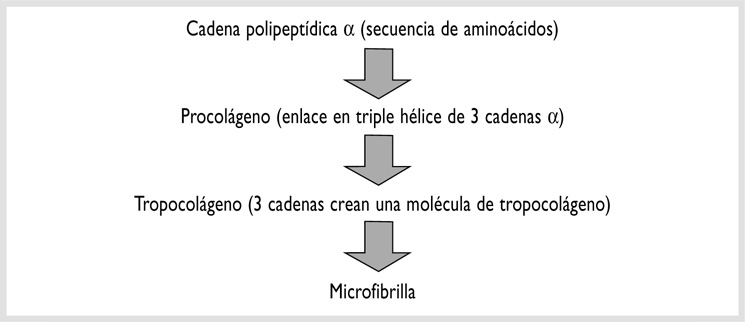
FIGURA 1-5.
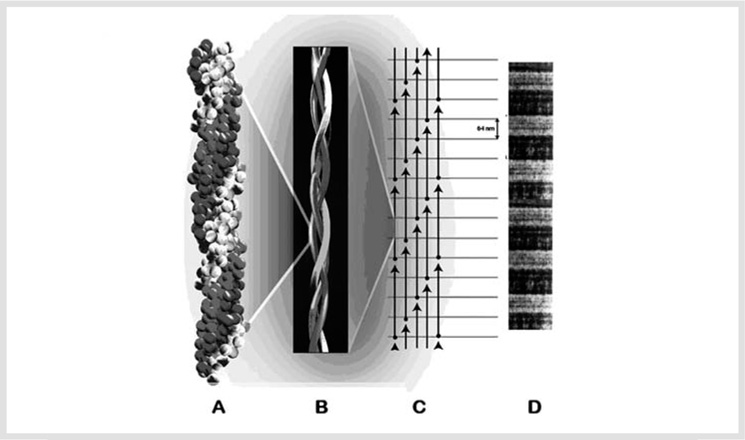
FIGURA 1-6. Representación esquemática de una fibrilla de colágeno tipo I: (A) aminoácidos se unen para formar una cadena α; la glicina ocupa las terceras posiciones (círculos negros); (B) y (C) tres cadenas α?forman la triple hélice de una molécula de colágeno; las cadenas α?están cubiertas por una fina capa de proteoglicanos y glucosaminoglicanos; (D) la molécula de colágeno se une para formar una molécula de tropocolágeno o microfibrilla; (E) microfibrilla o fibrilla de colágeno estriado; las microfibrillas están rodeadas por proteoglicanos y glucosaminoglicanos; (F) configuración de la red de fibrillas.
Todos los componentes del tendón, desde las cadenas de aminoácidos hasta la fibra de colágeno ya formada, se encuentran embebidos en el seno de la sustancia fundamental, la cual proporciona soporte a la estructura del tendón y a la vez sirve para la difusión de gases y nutrientes7 46.
El proceso extracelular se caracteriza por la unión entre moléculas y su posterior organización en estructuras fibrilares. En este proceso el colágeno adquiere sus propiedades mecánicas. El procolágeno es depositado en el espacio extracelular, cerca de la superficie de los fibroblastos. Varias moléculas de procolágeno se ensamblan para dar lugar a una nueva molécula corta y ligera que ahora se llama tropocolágeno (fig. 1-7). La molécula de tropocolágeno es el ladrillo básico en el edificio del colágeno53. Los procesos extracelulares incluyen enlaces cruzados entre moléculas y su organización en estructuras fibrilares, lo que confiere al colágeno su alta resistencia13 22 24. Así pues, 5 moléculas de tropocolágeno se agregan de manera superpuesta para formar una fibrilla de colágeno (fig. 1-7)53.
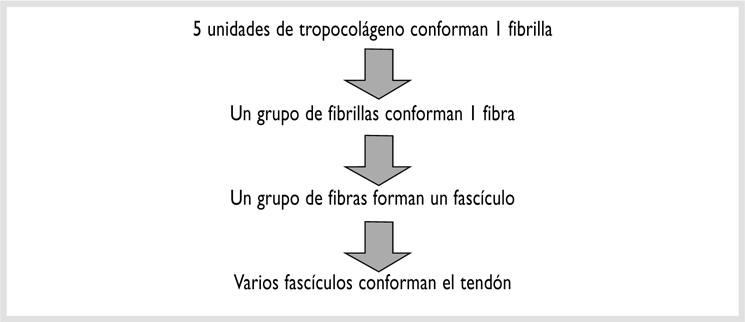
FIGURA 1-7.
Cada molécula de colágeno enlaza con su vecina, para lo cual invierte un cuarto de su longitud. Por último, las fibrillas de colágeno se agregan y se mantienen unidas gracias a la matriz para formar la fibra de colágeno, que es el próximo elemento en la estructura del tendón56.
La elastina contribuye a dar elasticidad al tendón. Son las responsables de devolver al tendón su configuración original ondulada tras ser estirado. Es una proteína no colágena que representa el 2% del peso seco del tendón23. Puede alargarse hasta un 70% de su longitud sin romperse46. Investigaciones recientes aseguran que está presente únicamente en el 10% de los tendones del individuo sano. En condiciones patológicas, como son las alteraciones hormonales, el número y volumen de las fibras elásticas tendinosas están claramente aumentados, pero en las heridas en proceso de curación se encuentran reducidos46.
La sustancia fundamental es un gel salino que otorga propiedades viscoelásticas al tendón y la lubrificación y el espacio necesarios para el deslizamiento y entrecruzamiento de los tejidos. Asimismo, es el medio para el aporte de nutrientes y gases.
Está compuesta por proteoglicanos, glicoproteínas –como la fibronectina, que une los fibroblastos a las fibras de colágeno– y agua, que dan lugar a GAG y PG.
La matriz extracelular la producen los fibroblastos. El agua representa el 70-80% del peso total, mientras que los proteoglicanos y glicoproteínas son el 1% del peso seco del tendón. El agua en este sistema está atrapada entre las cargas negativas de las moléculas de proteoglicanos, las cuales contienen un gran número de grupos hidroxilos que atraen el agua23 33 46. La matriz es constantemente remodelada por los fibroblastos y las enzimas degradantes, especialmente la colagenasa y proteoglicanasa.
La formación de tropocolágeno y matriz extracelular está íntimamente interrelacionada. Los proteoglicanos parecen regular la formación de fibrillas en la sustancia fundamental; la tasa de proteoglicanos disminuye en el tendón cuando el tropocolágeno ha madurado y alcanzado su tamaño final26.
La configuración geométrica del tendón es deudora de la función del músculo al cual está unido. La movilidad del tendón y la fuerza aplicada por el músculo determinan la orientación de las fibras de UMT en relación con el eje del tendón. Los músculos fusiformes son los que generan una mayor cantidad de fuerza sobre el tendón. Conforme aumenta la angulación de las fibras musculares con respecto al tendón, hay mayor disipación lateral de fuerza. Los tendones que en su recorrido sufren un cambio de dirección están sometidos a más tensión y su aporte vascular es menor debido a que soportan mayores fuerzas de compresión.
La disposición de las fibras de colágeno a lo largo del curso del tendón no es únicamente paralela. Por medio del microscopio polarizado se han encontrado hasta cuatro tipos de entrecruzamiento de fibras.
Las moléculas de tropocolágeno son estabilizadas y mantenidas unidas por medio de enlaces cruzados electrostáticos y químicos. Las moléculas poseen enlaces covalentes mediante puentes intramoleculares entre las cadenas α del mismo tropocolágeno e intermolecularmente entre moléculas de colágeno adyacentes. Los enlaces cruzados se encuentran dentro y entre las moléculas de colágeno, y las previenen de la rotura enzimática, mecánica o química12.
Los puentes derivan de reacciones enzimáticas en las que intervienen principalmente la lisina y la hidrolisina. La clave enzimática es la lisiloxidasa, que regula la tasa de puentes en el colágeno. Distintas cadenas de aminoácidos están conectadas por enlaces intermoleculares para formar fibrillas. Los enlaces son los responsables de la fuerza tensil del colágeno.
Los enlaces químicos se producen durante el metabolismo y su tasa disminuye con la edad. Los enlaces pueden ser reducibles o irreducibles. Los enlaces irreducibles se encuentran en el colágeno maduro, al que hacen más estable y fuerte. La reducción del número de enlaces hace al colágeno más débil. La hipertrofia del tendón se asocia con el aumento de la hidroxilación de la lisina en dos enlaces específicos localizados en el colágeno tipo I12 55.
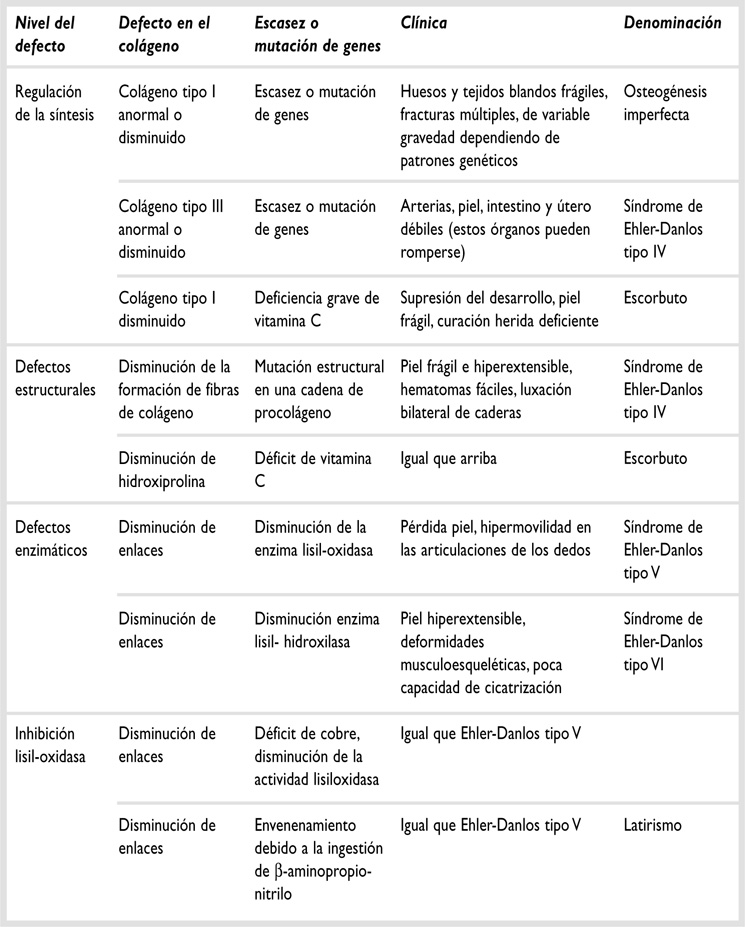
Existen muchas causas de defectos en el metabolismo del colágeno que pueden llegar a provocar trastornos clínicos. Entre ellas se cuentan las alteraciones genéticas, la osteogénesis imperfecta, el síndrome de Marfan o las condrodisplasias (tabla 1-3)21 22 50.
Las mutaciones genéticas disminuyen el número de enlaces y, por consiguiente, se produce un colágeno mucho más débil, que responde fácilmente a la elongación cuando se aplican pequeñas fuerzas. También pueden originar defectos en la estructura u organización del colágeno molecular. La gravedad del trastorno depende de la localización del gen mutado12.
Es más probable que el incremento de los enlaces ocurra en pacientes con diabetes. El resultado es un tejido duro que requiere más fuerza para ser estirado, de ahí la mayor incidencia de capsulitis retráctiles en pacientes con esta enfermedad43.
TABLA 1-3. Defectos del colágeno. Tomado de: Curwin SL. Tendon injuries: pathophysiology and treatment. En: Zachazewski JE, Magee DJ, Quillen WS. Athletic injuries and rehabilitation. Philadelphia:WB Saunders; 1996.
La unidad de menor tamaño en el tendón es el tropocolágeno, el cual, como se dijo, es una proteína compuesta por colágeno tipo I y creada por fibroblastos. Enlaces electrostáticos son responsables de la estabilidad intrínseca de estas moléculas, mientras que los enlaces cruzados entre moléculas de tropocolágeno facilitan que estas unidades se unan y formen fibrillas26.
Sólo ciertas zonas de algunos tendones de las manos y los pies poseen vaina, que, como se ha mencionado, posee dos capas. La vaina verdadera se encuentra en las zonas en las que existen un cambio de dirección y aumento de la fricción, por lo que se necesita una excelente lubricación. En cambio, la mayoría de nuestros tendones están rodeados por un tejido conectivo que recibe el nombre de paratendón. El colágeno del paratendón es de tipos I y III. El paratendón funciona como una funda elástica y permite el movimiento libre del tendón en los tejidos que lo rodean.
La unidad funcional menor del tendón son las fibrillas, las cuales se disponen en haces paralelos rodeados por sustancia matriz. Las fibras se agrupan en colecciones primarias de fibras encerradas dentro de tejido conectivo, que dan lugar al endotendón7. El endotendón es una red reticular de tejido conectivo dentro del tendón; se conoce también como haz primario. La unión de haces primarios con la inclusión de vasos, nervios y microsistema linfático conforma el fascículo o haz secundario. Los haces secundarios funcionan como verdaderas unidades independientes dentro del propio tendón. Varios haces secundarios constituyen el tendón, el cual se rodea de una fina capa llamada epitendón, que es la capa más externa del cuerpo del tendón7 13 26.
El epitendón es una red relativamente densa de colágeno. Esta red contiene fibras longitudinales, oblicuas y transversales. En estado de relajación parte de las fibras de colágeno del epitendón se encuentran formando un ángulo de 60º aproximadamente con las fibras del tendón. El ángulo decrece a 30º cuando el tendón se estira. El epitendón contiene el aporte vascular, nervioso y linfático31.
Un manojo de fibras tendinosas forma el haz primario de fibras –subfascículo– y grupos de estos haces forman haces secundarios –fascículos–. Un grupo de haces secundarios forman haces terciarios, los cuales, a su vez, forman el tendón. El endotendón rodea los haces primarios, secundarios y terciarios30 (fig. 1-8).
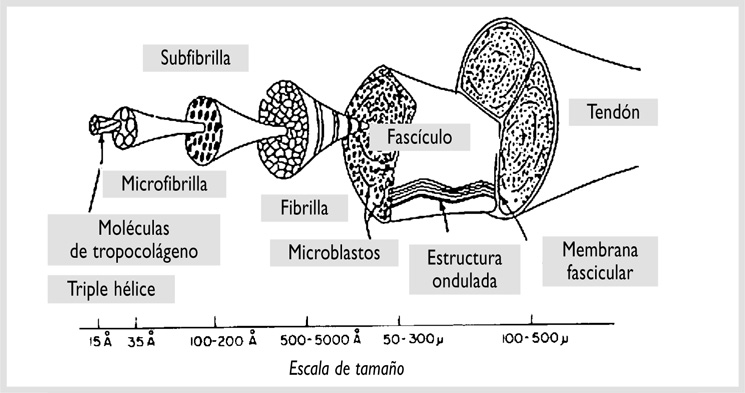
FIGURA 1-8. Jerarquía estructural del tendón desde las moléculas de tropocolágeno a la presentación final.Tomado de: Kastelic J, Galeski A, Baer E: The multicomposite structure of tendón. Connect Tissue Res 1978; 6(1):11-23.
El músculo y el tendón tienen un punto de encuentro donde se funden miofibrillas intracelulares con fibras extracelulares de colágeno. Esta zona de transición se denomina unión musculotendinosa (UMT) y constituye una unidad funcional única, capaz de adaptarse a las distintas situaciones de carga. La fuerza generada por el músculo se transmite a la UMT y al tendón, los cuales tienen que adaptarse al grado de solicitación para producir el movimiento correcto.
La UMT es una membrana plegada y extensa para aumentar la superficie de contacto y al mismo tiempo distribuir el estrés sobre dicha unidad. El ángulo que forma el tendón y el músculo es cercano a 0º, con la misma finalidad de disminuir la tensión sobre la unión.
La UMT es la placa de crecimiento del músculo debido a que las células que se adosan son capaces de generar colágeno; también es ésta la zona de crecimiento del tendón, capacidad que va disminuyendo conforme se acerca a la inserción en el hueso45. En esta región es donde se localizan los órganos de Golgi y los receptores nerviosos. La UMT es la zona de mayor sufrimiento al aplicar fuerzas de tracción durante la contracción muscular. Para paliar el estrés, las superficies en contacto presentan repliegues membranosos con el fin de aumentar dicha área de contacto52. La fortaleza de la UMT depende no solamente de la disposición anatómica de las superficies en contacto, sino que también interviene de manera decisiva la orientación de las fuerzas que confluyen en la propia UMT. Así, los tejidos en los que las fuerzas ejercen un cizallamiento sobre la unión, donde las fuerzas se aplican en paralelo a la superficie de la membrana, resultan más resistentes que las uniones en las que las fuerzas que provocan el estrés se aplican perpendicularmente a la membrana. El grado de contacto músculo-tendón disminuye enormemente después de una inmovilización articular28.
En el microscopio electrónico cabe observar los múltiples repliegues e invaginaciones que ofrece la membrana celular en la zona de unión a fin de aumentar la superficie de contacto y disminuir la tensión durante la fase de carga. El sarcolema de la última fila de células musculares es de morfología dentada, por lo que las fibras reticulares y colágenas entran en íntimo contacto con aquéllas (figs. 1-9a y 1-9b).
La UMT es, en definitiva, una zona crítica durante la aplicación de estrés mecánico, ya que en ella conviven dos elementos, músculo y tendón, que responden de manera muy diferente a dicho estrés. Además de las características materiales de los dos componentes de la unión, otro condicionante en la aparición de lesiones es el llamado efecto flecha, el cual somete a una igualdad asimétrica a dichos componentes52.
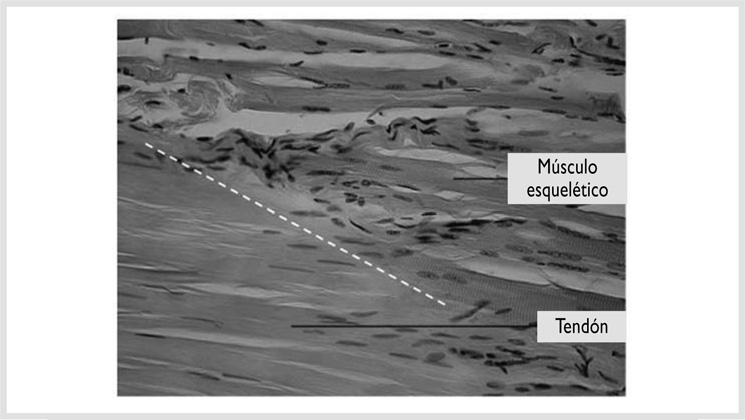
FIGURA 1-9a. Unión miotendinosa (400x). Tomado de: Departamento de Biología. Kilgore College. Texas, EE.UU.

FIGURA 1-9b. Unión miotendinosa.Tomado de: Departamento de Biología. Niagara County Community College. Nueva York, EE.UU.
La localización de la lesión en esta zona guarda relación con la actividad del músculo. Si la UMT se tensa con el músculo estimulado, la lesión acontece en la misma UMT. Si, por el contrario, se tensa con el músculo relajado, la lesión se alojará a poca distancia de la UMT.
Es la inserción gradual del tendón en el hueso o fibrocartílago. La transición de tejido blando a hueso sucede en un grosor de 1 mm, lo que dota a esta zona de una complejidad estructural considerable (fig. 1-10). La unión del tendón al hueso se denomina entesis.
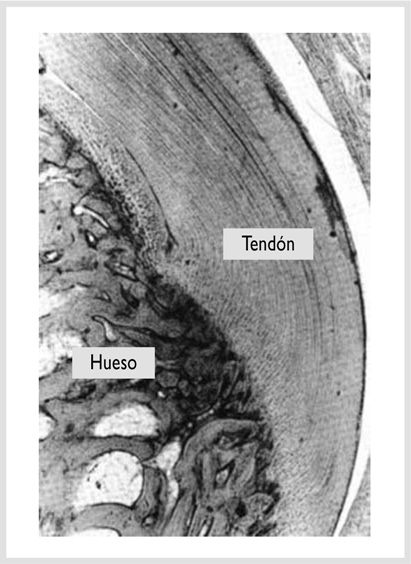
FIGURA 1-10. Unión osteotendinosa (40x). Tomado de: Rust TG. A Guide to Anatomy and Physiology Lab, 2 Ed. San Antonio: Southwest Educational Enterprises; 1986.
Recientemente se han descrito dos tipos de entesis: fibrosa y fibrocartilaginosa. Cada una de ellas se corresponde con una zona ósea determinada. Así, la entesis fibrosa ocurre en la diáfisis de los huesos largos, lo que Woo et al. denominan inserción indirecta; por otro lado, la entesis fibrocartilaginosa es típica de las epífisis de los huesos largos y se conoce como inserción directa58.
Directa: el tendón se inserta en el hueso formando un ángulo recto. La porción de transición presenta cuatro zonas: zona 1, similar al tendón; zona 2, de fibrocartílago, con células similares a los condrocitos; zona 3, de fibrocartílago mineralizado; zona 4, que corresponde al hueso.
Indirecta: la inserción en el hueso ocurre formando un ángulo agudo; la zona fibrocartilaginosa no existe y las fibras tendinosas se mezclan con el periostio rodeando el hueso.
La lesión suele localizarse en las proximidades de la UOT, pero rara vez sobre la misma unión. Se debe básicamente a las diferencias entre las propiedades materiales del tendón y el hueso.
En la entesis fibrocartilaginosa la porción de inserción da lugar a cuatro zonas de tejido fibroso puro que son: tendón, fibrocartílago desmineralizado, fibrocartílago mineralizado y hueso. Una característica de la UOT es que no existe vascularización en la zona de fibrocartílago3 10.
Los tejidos ligamentario y tendinoso están compuestos por fibroblastos, fibrocitos, fibras –tanto colágenas como elásticas y reticulares– y sustancia fundamental. Ambos actúan en un contexto similar, pues lo hacen en el seno de un complejo que implica su unión a otro tejido histológicamente diferente, bien hueso-ligamento-hueso, bien hueso-tendón-músculo-tendón-hueso. Esta transición tiene lugar en varias fases en las que el tendón/ligamento se transforma primero en fibrocartílago no mineralizado, después en fibrocartílago mineralizado y finalmente en hueso10.
Entre las propiedades mecánicas comunes más destacadas de tendones y ligamentos se encuentran la viscoelasticidad y la plasticidad, dependientes del número de enlaces de colágeno inter e intramoleculares, de la relación de formas solubles/insolubles de colágeno y del contenido en agua54. Difieren en cuanto a la cantidad de enlaces cruzados y colágeno tipo I, que es mayor en los tendones, en contraste con una mejor vascularización de los ligamentos (tabla 1-4).
TABLA 1-4. Semejanzas y diferencias entre ligamentos y tendones.
Semejanzas |
Diferencias |
Densidad, empaquetado en haces cerrados. |
Los tendones poseen algunas células propias. |
Forma ondulada en reposo. |
Los tendones tienen los haces más alineados. |
Células entre los haces de fibras. |
Los tendones poseen más colágeno tipo I. |
Tasa metabólica relativa baja. |
Los tendones poseen más enlaces cruzados. |
Aporte sanguíneo relativo escaso. |
El aporte sanguíneo es mayor en los ligamentos. |
1. Astrom M. Laser Doppler flowmetry in the assessment of tendon blood flow. Scand J Med Sci Sports 2000; 10(6):365-7.
2. Backman C, Friden J, Widmark A. Blood flow in chronic Achilles tendinosis. Radioactive microsphere study in rabbits. Acta Orthop Scand 1991; 62(4):386-7.
3. Benjamin M, Qin S, Ralphs JR. Fibrocartilage associated with human tendons and their pulleys. J Anat 1995; 187 (Pt 3):625-33.
4. Benjamin M, Ralphs JR. Tendons and ligaments—an overview. Histol Histopathol 1997; 12(4):1135-44.
5. Boushel R, Langberg H, Green S, Skovgaard D, Bulow J, Kjaer M. Blood flow and oxygenation in peritendinous tissue and calf muscle during dynamic exercise in humans. J Physiol 2000; 524 (Pt 1):305-13.
6. Bray RC. Blood supply of ligaments. Orthop Int 1995; 3:38-48.
7. Butler DL, Grood ES, Noyes FR, Zernicke RF. Biomechanics of ligaments and tendons. Exerc Sport Sci Rev 1978; 6:125-81.
8. Clark MG, Clerk LH, Newman JM, Rattigan S. Interaction between metabolism and flow in tendon and muscle. Scand J Med Sci Sports 2000; 10(6):338-45.
9. Cook CS, McDonagh MJ. Measurement of muscle and tendon stiffness in man. Eur J Appl Physiol Occup Physiol 1996; 72(4):380-2.
10. Cooper RR, Misol S. Tendon and ligament insertion. A light and electron microscopic study. J Bone Joint Surg Am 1970; 52(1):1-20.
11. Culav EM, Clark CH, Merrilees MJ. Connective tissues: matrix composition and its relevance to physical therapy. Phys Ther 1999; 79(3):308-19.
12. Curwin SL. The aetiology and treatment of tendinitis. In: Harries M, Williams C, Stanish WD, Michelis LJ. Oxford Textbook of Sports Medicine. Oxford: Oxford University Press; 1994.
13. Curwin SL. Tendon injuries: Pathophysiology and treatment. In: Zachazewski JE, Magee DJ, Quillen WS. Athletic injuries and rehabilitation. Philadelphia: WB Saunders; 1996.
14. Curwin SL, Roy RR, Vailas AC. Regional and age variations in growing tendon. J Morphol 1994; 221(3):309-20.
15. Eiken O, Rank F. Experimental restoration of the digital synovial sheath. Scand J Plast Reconstr Surg 1977; 11(3):213-8.
16. El Hawary R, Stanish WD, Curwin SL. Rehabilitation of tendon injuries in sport. Sports Med 1997; 24(5):347-58.
17. Elliot DH, Crawford GNC. The thickness and collagen content of tendon relative to the strength and cross-sectional area of muscle during growth. Proc Roy Soc B 1965; 162:198-202.
18. Freeman MA, Wyke B. The innervation of the knee joint. An anatomical and histological study in the cat. J Anat 1967; 101(3):505- 32.
19. Gelberman RH. Flexor tendon physiology: tendon nutrition and cellular activity in injury and repair. Instr Course Lect 1985; 34:351-60.
20. Gross M. Chronic tendinitis: Pathomechanics of injury, factors affecting the healing response, and treatment. J Orthop Phys Ther 1992; 16(6):248-61.
21. Hayem G. Histoire naturelle pathologie tendineuse. Kinesit Scient 2000; 404:8-9.
22. Herzberg G, Gregoire O, Comtet JJ. Anatomie et physiologie du tendon normal. Ency Med Chir 140007-A10-6, 1985.
23. Hess GP, Cappiello WL, Poole RM, Hunter SC. Prevention and treatment of overuse tendon injuries. Sports Med 1989; 8(6):371-84.
24. Ippolito E, Postacchini F. Anatomia. In: Perugia L, Postacchini F, Ippolito R. I tendini, biologia, patologia, clinica. Milán. Masson; 1985.
25. Jozsa L, Balint J, Kannus P, Jarvinen M, Lehto M. Mechanoreceptors in human myotendinous junction. Muscle Nerve 1993; 16(5):453-7.
26. Jozsa L, Kannus P. Human tendons: Anatomy, physiology, and pathology. Champaign: Human Kinetics; 1997.
27. Jozsa L, Kannus P, Jarvinen TA, Balint J, Jarvinen M. Number and morphology of mechanoreceptors in the myotendinous junction of paralysed human muscle. J Pathol 1996; 178(2):195-200.
28. Kannus P, Jarvinen TL, Sievanen H et al. Effects of immobilization, three forms of remobilization, and subsequent deconditioning on bone mineral content and density in rat femora. J Bone Miner Res 1996; 11(9):1339-46.
29. Kannus P, Renstrom P. Treatment for acute tears of the lateral ligaments of the ankle. Operation, cast, or early controlled mobilization. J Bone Joint Surg Am 1991; 73(2):305-12.
30. Kastelic J, Galeski A, Baer E. The multicomposite structure of tendon. Connect Tissue Res 1978; 6(1):11-23.
31. Khan KM, Cook JL, Bonar F, Harcourt P, Astrom M. Histopathology of common tendinopathies. Update and implications for clinical management. Sports Med 1999; 27(6):393-408.
32. Kirkendall DT, Garrett WE. Function and biomechanics of tendons. Scand J Med Sci Sports 1997; 7(2):62-6.
33. Kischer CW, Speer DP. Microvascular changes in Dupuytren’s contracture. J Hand Surg [Am] 1984; 9A(1):58-62.
34. Kvist M, Hurme T, Kannus P et al. Vascular density at the myotendinous junction of the rat gastrocnemius muscle after immobilization and remobilization. Am J Sports Med 1995; 23(3):359-64.
35. Leadbetter WB. Cell-matrix response in tendon injury. Clin Sports Med 1992; 11(3):533-78.
36. Leversedge FJ, Ditsios K, Goldfarb CA, Silva MJ, Gelberman RH, Boyer MI. Vascular anatomy of the human flexor digitorum profundus tendon insertion. J Hand Surg [Am] 2002; 27(5):806-12.
37. Lohr JF, Uhthoff HK. The microvascular pattern of the supraspinatus tendon. Clin Orthop 1990; (254):35-8.
38. Lundborg G, Holm S, Myrhage R. The role of the synovial fluid and tendon sheath for flexor tendon nutrition. An experimental tracer study on diffusional pathways in dogs. Scand J Plast Reconstr Surg 1980; 14(1):99-107.
39. Magnusson SP, Hansen P, Kjaer M. Tendon properties in relation to muscular activity and physical training. Scand J Med Sci Sports 2003; 13(4):211-23.
40. Manske PR, Lesker PA. Flexor tendon nutrition. Hand Clin 1985; 1(1):13-24.
41. Mayer L. The physiological method of tendon transplantation. Surg Gynecol Obstet 1916; 22:183-97.
42. McLatchie GR, Lennox CME. The soft tissues: trauma and sports injuries. Boston: Butterworth Heinemann; 1993.
43. Monnier VM, Vishwanath V, Frank KE, Elmets CA, Dauchot P, Kohn RR. Relation between complications of type I diabetes mellitus and collagen-linked fluorescence. N Engl J Med 1986; 314(7): 403-8.
44. Nakamura N, Hart DA, Frank CB et al. Efficient transfer of intact oligonucleotides into the nucleus of ligament scar fibroblasts by HVJ-cationic liposomes is correlated with effective antisense gene inhibition. J Biochem (Tokyo) 2001; 129(5):755-9.
45. Noonan TJ, Garrett WE Jr. Injuries at the myotendinous junction. Clin Sports Med 1992; 11(4):783-806.
46. O’Brien M. Functional anatomy and physiology of tendons. Clin Sports Med 1992; 11(3):505-20.
47. Prockop DJ, Guzman NA. Collagen diseases and the biosynthesis of collagen. Hosp Pract 1977; 12(12):61-8.
48. Rathbun JB, Macnab I. The microvascular pattern of the rotator cuff. J Bone Joint Surg Br 1970; 52(3):540-53.
49. Smith JW. Blood supply of tendons. Am J Surg 1965; 109:272-6.
50. Stanish WD, Curwin SL, Mandell S. Tendinitis: its etiology and treatment. Lexington: Collamore Press; 1984.
51. Teitz CC. Scientific Foundations of Sports Medicine. Philadelphia: Decker; 1989.
52. Tidball JG, Chan M. Adhesive strength of single muscle cells to basement membrane at myotendinous junctions. J Appl Physiol 1989; 67(3):1063-9.
53. Tillman LJ, Chasan NP. Properties of dense connective tissue and wound healing. In: Hertling D, Kessler RM. Management of common musculoskeletal disorders. Philadelphia: Lippincott Williams & Wilkins; 1996.
54. Tipton CM, Matthes RD, Maynard JA, Carey RA. The influence of physical activity on ligaments and tendons. Med Sci Sports 1975; 7(3):165-75.
55. Tuite DJ, Renstrom PA, O’Brien M. The aging tendon. Scand J Med Sci Sports 1997; 7(2):72-7.
56. Viidik A. Functional properties of collagenous tissues. Int Rev Connect Tissue Res 1973; 6:127-215.
57. Wahl SM, Renstrom P. Fibrosis in soft tissue. In: Leadbetter WB, Buckwater JA, Gordon SI. Sports-induced inflammation. Park Ridge: AAOS; 1990.
58. Woo SL, Maynard J, Butler D, Lyon R, Torzilli P, Akeston W. Ligament, tendon, and joint capsule insertions to bone. In: Woo SL, Buckwalter JA. Injury and repair of the musculoskeletal soft tissues. Park Ridge: AAOS; 1988.
59. Zimny ML, DePaolo C, Dabezies E. Mechano-receptors in the flexor tendons of the hand. J Hand Surg [Br] 1989; 14(2):229-31.