Este manual tiene por objetivo la adquisición de todos los fundamentos básicos y comunes para el desarrollo de un trabajo eficiente, regularizado, competente y seguro en lo que se refiere al ámbito de las industrias química, biológica y farmacéutica.
La industria química sufre un continuo cambio por la innovación gracias a la investigación y el desarrollo (I+D) y sus avances técnicos, provocando que las operaciones en un laboratorio disten mucho de aquellas antiguas operaciones de vidrio, siendo hoy en día necesaria una alta capacitación para el desarrollo del trabajo de campo. En este sentido, se hace aún más necesaria la constante formación y el entrenamiento en la capacitación de los profesionales competentes.
A lo largo de este capítulo, se tratará de los distintos procesos que se realizan en un laboratorio y, posteriormente, son llevados a la industria. Se van a tratar desde un punto de vista teórico, basándose en las variaciones de sus parámetros físicos y químicos, con los principios universales de equilibrio que los rigen.
A continuación, se mostrarán las operaciones básicas características y sus aplicaciones más importantes en la industria.
2.1. Concepto. Definición
Cuando se habla de operaciones básicas, estas se refieren a aquellas operaciones comunes realizadas, basadas en procesos físicos y químicos, que se llevan a cabo en las distintas industrias. Dichas operaciones se centran en el movimiento de materia o flujo, sin que se produzca ningún tipo de reacción química, en un estado llamado estacionario, es decir, donde las propiedades se mantienen constantes en el tiempo.
Por ello, se definen las operaciones básicas o unitarias como aquellos conjuntos de procesos, de carácter tanto físico como químico, aplicados a una determinada cantidad de materia determinada.
2.2. Clasificación de las operaciones unitarias
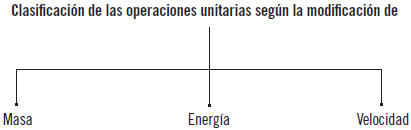
Las operaciones básicas tienen por objeto la modificación de alguno de sus parámetros. Estos pueden ser de materia, energía o movimiento, clasificándose en función de la transferencia de estos parámetros entre dos sistemas distintos. No obstante, la transferencia puede implicar uno o varios parámetros, obteniendo la siguiente clasificación, en función de:

Es importante, a la hora de entender estos procedimientos, que se produce una transferencia de cualquier parámetro de uno a otro sistema, de modo que siempre la suma de ambos sea constante.

Nota
Las operaciones básicas son aquellos procesos simples llevados a cabo en un laboratorio.
De transferencia de materia
Son aquellas operaciones en la que existe un trasvase físico de materia entre dos sistemas cualquier. El cuerpo humano produce un sistema de transferencia de materia continuo, como es la respiración: se toma oxígeno del exterior y se expulsa dióxido de carbono. Se transfieren dos sustancias materiales entre los dos sistemas, cuerpo y medioambiente.
Así, cuando se presentan dos sistemas con una diferencia en su composición, tienden a intercambiar materia hasta alcanzar una situación de equilibrio.

Sabía que...
La prueba del carbono 14, que determina la edad de los distintos organismos, se basa en establecer cuándo finaliza la transferencia de carbono entre el organismo y el medio donde vive.
Volviendo al ejemplo del cuerpo humano, si no hubiera esa diferencia de oxígeno y dióxido, no se podría producir la respiración, ya que si se está rodeado de dióxido, no hay intercambio de oxígeno y, por lo tanto, sin respiración,se produciría la consiguiente muerte del organismo.
De transferencia de energía
Son aquellas operaciones en la que existe un paso de energía entre dos sistemas cualesquiera, donde el proceso de transferencia entre dos cuerpos, por la distinta temperatura, se denomina calor.

Sabía que...
Unos de los principales avances de la química en el siglo XX fue pensar en que no se puede crear algo de la nada, si no transformar los parámetros del esquema.
Esta transferencia de energía se usa principalmente para el aumento o disminución de la temperatura de los cuerpos, es decir, ambos cuerpos no pueden aumentar su temperatura o viceversa, siendo este uno de los principios básicos de la física.

Nota
Las operaciones básicas son procesos elementales a los que es sometida la materia.
De este modo, la transferencia energética se produce a través de un medio o directamente, por lo que es importante determinar el proceso.

Nota
Se ha de tener en cuenta que en física no existe el concepto de frío, y la transmisión de energía tal como se conoce es denominada transferencia de energía en forma de calor o simplemente calor.
Cuando dicha transferencia se produce a lo largo de un medio, este influye en el proceso, facilitando o entorpeciendo la transmisión,existiendo medios:
Ejemplo: Se usan suelos de parquet para que la energía no se transmita al suelo y no disminuya la energía de la habitación.
Ejemplo: Se usan recipientes de aluminio para conservar los helados en el refrigerador.
De transmisión simultánea de materia y energía
En este tipo de fenómenos, se produce un contacto físico íntimo entre los elementos o fases que se disponen en el sistema. Cuando esas fases se unen, comienza un intercambio tanto de energía como de materia.

Ejemplo
Si se quema leña, se observa el tronco ceder calor al medio, a la vez que cede parte de su materia en forma de gas, quedando unas pocas cenizas.
En cambio, si ahora se fija como referencia el medio externo, por ejemplo una habitación, esta toma dióxido y energía para aumentar su temperatura.

Recuerde
Estos fenómenos se producen cuando existe contacto físico entre los elementos o fases.
De transporte de cantidad de movimiento
En el caso de disponer de un sistema material o fase, se le puede aplicar una variación en su movimiento para producir una variación de algunos de sus componentes.
Este transporte, por cantidad de materia, cuando se pone en contacto con dos sustancias, con distintas velocidades y debido al contacto entre estas fases, alcanza la misma velocidad por el rozamiento de ambos fluidos, produciendo la situación de equilibrio e igualando sus velocidades.

Importante
La interacción por rozamiento es el fundamento para las operaciones básicas de sustancias tanto fluidas como sólidas.
Debido a que se produce la interacción entre sólidos y fluidos, se puede hacer la siguiente clasificación, según sean las dos fases que intervienen:

Nota
El transporte de cantidad de movimiento se clasifica en tres tipos:
Complementarias
Se llama operación complementaria a aquel tipo de operación usada en la industria que no se incluye en los apartados anteriores. Son procesos previos a la realización de los anteriores, como la adecuación de algunas características necesarias para proceder a aplicar alguno de los procesos anteriores. Ejemplo de ellas son: molido, tamizado, pulverizado, disolución, etc.

Nota
La operación complementaria es un tipo de operación utilizado para la preparación de algún tipo de muestra o como afín de las sustancias que son de utilidad y necesarias para este tipo de ensayo.
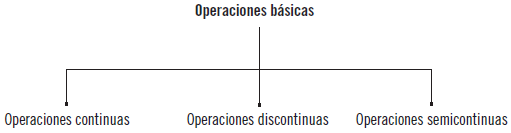
Operaciones continuas, discontinuas y semicontinuas
Si se desea transformar cualquier sustancia en un proceso de trasformación, se le debe aplicar más de un tipo de proceso. Este es el argumento principal de esta nueva clasificación de las operaciones básicas: cuando un proceso se lleva a cabo en un único paso, es denominado como continuo y, si este se lleva a cabo con interrupciones en algunas de las variables, es denominado discontinuo.
De este modo, se obtiene la siguiente clasificación:
Balances de materia
El universo se rige por los principios básicos basados en la conservación.
No es algo nuevo, ya que Anaxágoras lo expresaba de este modo ya por el año 450 a. C.: “nada se crea ni desaparece, sino que las cosas ya existentes se combinan y luego de nuevo se separan”.
En lo que se refiere a la materia, esto es igualmente aplicable. Este principio dice lo siguiente: “la cantidad de materia inicial es igual a la cantidad de materia final a lo largo de un proceso químico”.
En este sentido, cuando se habla de materia, se ha de hablar cuantitativamente de masa. Por lo tanto, siempre que se quiera comprobar cualquier proceso, basta con conocer si la suma de la masa de la materia inicial es igual a la materia final y comprobar la diferencia. Cuanto menor sea la diferencia, mejor se habrá optimizado el proceso.

Definición
Masa
Cantidad de materia que posee un cuerpo.
Leyes que regulan el proceso
La ley principal que rige el proceso es la Ley de Conservación de la Masa, la cual establece que, en un sistema cerrado, la masa del mismo se mantiene constante. Esto, hoy en día, se establece en una serie de salvedades basadas en la Teoría de la Relatividad de Einstein. Estas salvedades son:
De esta forma, cuando se habla de fluidos, resulta más sencillo establecer una ley derivada de la anterior, tomando en este caso parámetros volumétricos.

Sabía que...
Si se observa por ejemplo la combustión de una cerilla, visiblemente se aprecia que no se cumple el principio de conservación de la materia. No fue hasta 1785 cuando Antoine Lavoisier enunció que la masa del inicio del proceso es igual a la masa del final del proceso.
Flujo másico y volumétrico
Dentro de la industria, los fluidos se mueven a través de distintos dispositivos, principalmente tuberías o toberas.
Los distintos materiales que son trasportados se pueden medir. Esto se hace mediante la determinación de distintas magnitudes:

Recuerde
Según la Ley de Conservación de la Masa, en un sistema cerrado, la masa del mismo se mantiene constante.
Ambas magnitudes tienen una magnitud fundamental que las relaciona, denominada densidad. Según sea su utilidad, se transformará en una magnitud o en otra. Debido a esta relación directa, se pueden usar los mismos dispositivos de medición, llamados caudalímetros:

Ejemplo
Una ambulancia suena más aguda cuando se acerca y más grave cuando se aleja.
No obstante, no se puede utilizar un único dispositivo de medida, por lo que en la industria se encuentra una gran variedad de ellos. Llegar a conocer su funcionamiento es primordial a la hora de usarlos y tomar medidas.

Recuerde
Se miden tanto flujos de masas como de volúmenes. Ambos están relacionados por la densidad de la sustancia, aplicando según qué método, a partir de las propiedades de la sustancia.
Debido a la enorme complejidad de procesos físico-químicos llevados a cabo en la industria, es importante introducir un apartado donde se expliquen aquellos más comunes. Por ello, a continuación se describirá el proceso y sus fundamentos físicos y químicos, para entender mejor este y poder llevar a cabo las posibles modificaciones, facilitando el aprendizaje técnico.
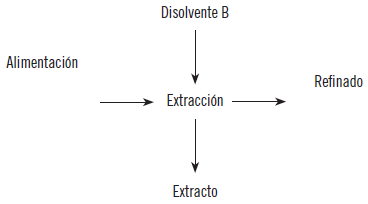
3.1. Extracción
Es un procedimiento de separación que consiste en el uso de disolvente selectivo (disolvente que únicamente actúa sobre unas sustancias de características determinadas y no sobre otras). De este modo, se separan distintas sustancias que pertenecen a una mezcla.
Esta separación se produce cuando las sustancias son disueltas por la fase líquida. Esta sustancia se extrae de su fase inicial; puede estar en un estado sólido o disuelto (dicha disolución puede resultar a partir de un sólido, de un líquido o de un gas cualquiera).
Asimismo, es importante conocer el proceso de disolución, definiéndolo como una mezcla homogénea donde, a simple vista, no se distingue ninguno de los componentes, de dos o más sustancias. Está compuesta de:

Ejemplo
Si se disuelven unos pocos gramos de sal en un litro de agua, se hablaría de disolvente para referirse al agua y de soluto para hablar de la sal.
Por otro lado, el disolvente más importante del que se dispone, además del más utilizado, es el agua, siendo sus disoluciones denominadas disoluciones acuosas. Por ello, se dice que el agua es el disolvente universal, ya que disuelve grandes cantidades de un enorme número de sustancias.
Para poder trabajar con disoluciones, es necesario saber su composición y su concentración. Para ello, se puede seguir la siguiente fórmula:
C (g/l) = m (g)/v (l)

Aplicación práctica
Usted se encuentra en un laboratorio, es necesario utilizar 30 g de un soluto y solo se dispone de tres disoluciones, a, b y c. ¿Qué cantidad de cada una de las disoluciones usaría para disponer de esos 30 g de soluto?
SOLUCIÓN
Para obtener 30 g de soluto utilizando la primera disolución, tomando 3 l, 3 l con cada litro que contiene 10 g da un total de 30 g, por lo que esta disolución es correcta.
Para obtener 30 g de soluto utilizando la segunda disolución, tomando 6 l, 6 l con cada litro que contiene 5 g da un total de 30 g, por lo que esta disolución es correcta.
Para obtener 30 g de soluto utilizando la tercera disolución, tomando 2 l, 2 l con cada litro que contiene 15 g da un total de 30 g, por lo que esta disolución también es correcta.
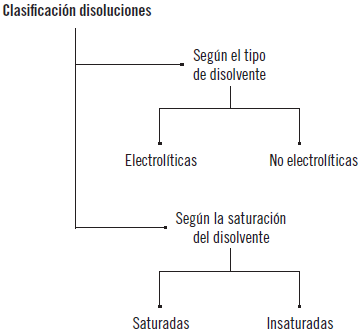
Por otro lado, las disoluciones se pueden clasificar en dos grandes grupos:
Aunque, como parámetro operativo de una disolución, es necesario determinar si la disolución es:
Líquido-líquido
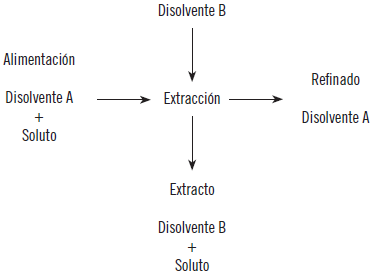
La extracción líquido-líquido es un proceso de extremada importancia en la separación de mezclas homogéneas líquidas. Este proceso es utilizado principalmente en la separación de las sustancias que forman parte de una disolución, mediante la transferencia de sus solutos a otra disolución o fase inmiscible (no son solubles entre ambas). Esta extracción de la fase inicial se consigue mediante el contacto físico directo entre las dos fases, por lo que se produce asociada a fenómenos de agitación, para aumentar la superficie de contacto entre fases y mejorar el rendimiento en la materia trasferida.
Existen dos tipos de extracción:

Recuerde
Concentración es masa de soluto partido por el volumen de disolvente.
La extracción se produce por un proceso denominado transferencia de materia, por desplazamiento de los componentes de una mezcla a otra, determinado por la capacidad de disolverse en cada una de la fases o miscibilidad. La mayor solubilidad de una de las sustancias provoca que los elementos sometidos a extracción difundan de una fase a la otra. En este sentido, un parámetro útil para determinarla es el coeficiente de distribución de fases.

Recuerde
La extracción puede ser simple o continua. Además, dicho proceso se produce mediante la transferencia de materia.
Por otro lado, es interesante conocer cuáles son los parámetros que influyen en el proceso de extracción, para mejorar el rendimiento, ya que no son muy altos, por lo que se repite el proceso para obtener altos rendimientos. Estos parámetros son:
K = [Afase1] / [Afase2]
Como se observa, en la siguiente gráfica aparecen todos los comportamientos posibles. El más habitual es la variación lineal representada por una línea roja (cuando aumenta la temperatura aumenta la solubilidad).Hay también comportamientos muy anormales, como el representado por la línea azul marino, en el que no se observa ningún patrón.
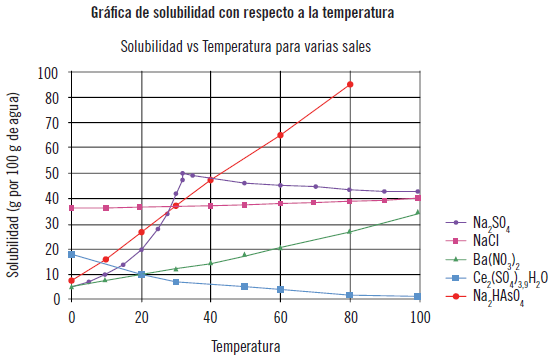
Respecto a los tipos de extracción líquido-líquido, se señalan los siguientes:
Por otro lado, se encuentran las extracciones en la industria, donde la implantación de la operación de extracción líquido-líquido a gran escala en procesos industriales es una operación relativamente nueva, con respecto al resto de técnicas(destilación y absorción). No obstante, se ha convertido en un proceso de enorme importancia.
En este caso, la extracción líquido-líquido se ha ido desarrollando por la alta demanda de productos nuevos y la mejora de los procesos y el alto desarrollo de los disolventes específicos.

Recuerde
La extracción depende de la solubilidad y la miscibilidad y el coeficiente depende de la temperatura.
Esta técnica denota su gran importancia por su aplicación en la industria petrolera, debido a que mejora los rendimientos y permite la extracción de un mayor número de sustancias provenientes del crudo, cada día más escasas y valiosas.
Ejemplos de extracción líquido-líquido son:
A modo de resumen, puede decirse que la extracción líquido-líquido es un proceso de separación de extremada importancia en la separación de mezclas homogéneas líquidas. Existen dos tipos: simple y continua. Asimismo, la extracción se produce por un proceso denominado transferencia de materia. Los parámetros que influyen en el proceso de solubilidad son: composición, temperatura, miscibilidad y coeficiente de distribución.
A continuación, se presenta un ejemplo con el que clarificar este apartado.
Ejemplo de distribución
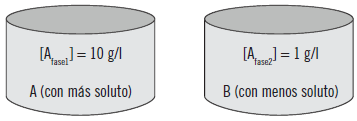
Se dispone de una sustancia A con un K= 10, es decir, que cuando se ponen en contacto dos fases que disponen de un componente común A, transcurrido un cierto tiempo, la relación entre ambas es de 10.
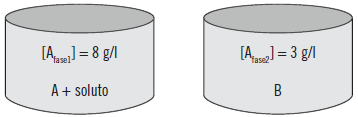
Si se dispone de dos fases, una fase 1 de 8 g/l de concentración y otra fase 2 de 3 g/l.
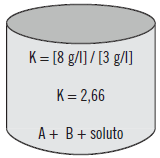
Se unen y alcanzado el equilibrio, cumplen la proporción de K=10 de la siguiente forma.
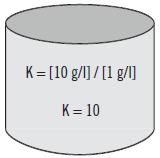
De la fase 2, se han trasferido 2 g a la fase 1, alcanzando el equilibrio determinado numéricamente por K=10. Seguidamente, al ser inmiscibles los disolventes, se separan mediante decantación y se obtiene dicho extracto.
Sólido-líquido
Este en un tipo de extracción donde intervienen dos fases, una de las cuales es sólida y la otra líquida. También se conoce con el nombre de lixiviación. Es una operación unitaria muy usada a nivel doméstico.

Ejemplo
Cuando se prepara un té o un café, se realiza la extracción de una sustancia (cafeína) contenida en un sólido (café molido) con una sustancia líquida(agua). Se produce por contacto de los dos elementos a altas temperaturas.
Su fundamento es el de la disolución selectiva. Como se explicó anteriormente, se produce una disolución selectiva de diversos componentes de la muestra sólida, obteniendo una disolución nueva y un soluto sin parte de algunos de sus componentes.

Ejemplo
Si se vuelve al ejemplo del café molido, al final del proceso, por una parte, se dispone de una disolución formada por cafeína y agua y, por otra, el resto del café sin parte de cafeína, que le ha sido extraída.
Uno de los procesos más simples dentro de un laboratorio, es la denominada percolación, que no es más que hacer fluir un disolvente a lo largo de un sólido (se fuerza el fluir del disolvente a través de la muestra en un lecho fijo).
Para conseguir una extracción lo más rápida y eficiente de la fase sólida y poder disponer de una superficie lo más grande posible, se produce el triturado de la muestra sólida, de forma que se favorezca el fluir del disolvente dentro de la muestra.
Las variables que influyen en este proceso son las siguientes:

Aplicación práctica
Hacer café es una extracción sólido-líquido. Comente las variables que influyen en la extracción de cafeína. Hágalo teniendo en cuenta los siguientes parámetros:
SOLUCIÓN
La cafeína no se extrae de forma directa, si no que hay que variar algunos parámetros.
Tipos de extracción
Respecto a los tipos de extracción, se pueden señalar los que se describen a continuación.
Extracción Soxhlet
Es el tipo de extracción más simple que se puede encontrar dentro de esta clasificación. Para proceder a dicha extracción, se toma un matraz donde se calienta el disolvente hasta su estado de ebullición, de forma que este sea lo más puro posible. A continuación, se refrigera el disolvente para producir el contacto entre la fase sólida y la fase líquida. Para la realización de dicho dispositivo, es necesario:
El proceso es cíclico, por lo que el disolvente está constantemente evaporándose y licuándose, de forma que existe un flujo continuo de disolvente a través de la muestra, el cual no lleva ninguna cantidad de soluto.
Como se observa, es un proceso conceptual e instrumentalmente muy simple, el cual produce altos rendimientos en la recuperación de extractos, aunque como inconvenientes serían mencionables la gran lentitud y el enorme gasto de disolvente.
Finalmente, este proceso se completa mediante una operación complementaria, denominada concentración por evaporación, donde se elimina la mayor parte del disolvente, quedando el extracto lo más concentrado posible.

Equipo de extracción Soxhlet industrial
Extracción por ultrasonidos
Es una mejora del proceso más simple. Se lleva a cabo mediante la unión de las dos fases, la sólida y la líquida, en un recipiente en la que se fuerza la disolución del extracto mediante ultrasonidos. Es una forma barata de disolver muestras.

Definición
Ultrasonidos
Sonidos cuya frecuencia es inaudible para el oído humano y de magnitud muy alta.
Como este medio es un disolvente, pueden formarse burbujas, las cuales, en su proceso de formación, dilatan o explotan violentamente, aumentando la presión y la temperatura de forma localizada en el sustrato. Debido al aumento de temperatura mediante el proceso de sonicación, se genera una agitación que provoca la transferencia de masa como soluto.

Sonicador del Instituto Weizmann de Ciencia
Extracción por microondas
Las microondas son un tipo de frecuencia de onda muy baja y tienen la propiedad de interferir con ciertas partículas, aumentando su movimiento sobre sí mismas y sobre el global del sistema y, por lo tanto, también aumenta su temperatura.
Asimismo, el extractor de microondas está compuesto por:
Es un método rápido, que produce la agitación y extracción a la misma vez y, además, es de bajo consumo en los disolventes que se utilizan.

Extractor por microondas
A continuación, se presentan una serie de ejemplos que se suelen utilizar en el área de la industria.

Recuerde
En el proceso de extracción sólido-líquido pueden influir las siguientes variables: relación disolvente sólido, pH, temperatura y método de agitación.
Extracción de azúcar en la remolacha
El azúcar se extrae de la remolacha azucarera y de la caña de azúcar a través de un proceso natural mediante extracción sólido-líquido. El azúcar es una sustancia que aparece en la raíz de la remolacha y en la propia caña de azúcar.
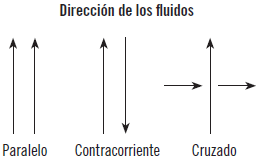
La raíz de la remolacha, en la fábrica, es pretratada cortándose en tiras para mejorar la superficie de contacto. A continuación, se produce el proceso de extracción de la sacarosa, comúnmente llamada azúcar, lo que se realiza haciendo fluir el disolvente, agua, a contracorriente a lo largo de las cañas de azúcar, en unas condiciones determinadas de pH y temperatura. Por último, se somete a un proceso de refinamiento de la sustancia, dando lugar al azúcar de uso doméstico.
Lixiviación de oro
El tratamiento metalúrgico de las menas de oro está basado principalmente en las propiedades inusuales del oro. Este elemento es de los más estables que existen en la naturaleza. Cuando el oro aparece asociado a otros elementos en sus menas, puede ser extraído por extracción sólido-líquido, donde el disolvente es una disolución acuosa de cianuro. Es un método bastante antiguo, en el cual se amontonan las distintas menas en forma de pila. El mineral fracturado se coloca sobre una base impermeable, de forma que, sobre la parte superior de la pila, se vierte la disolución de cianuro, produciéndose el fenómeno de percolación, disolviendo los metales preciosos contenidos en la mena. Así, la disolución enriquecida de oro y plata se recoge sobre la base impermeable. Finalmente, el oro se puede extraer mediante la adición de carbón activado o carbón en polvo, y posteriormente, se produce la filtración.
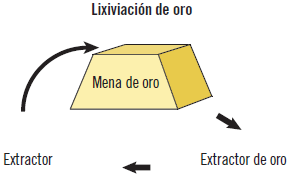
La flecha de la parte inferior indica que la misma disolución que ha fluido a lo largo de la mena se filtra el oro, volviendo como agente extractor regenerado. De esta forma, se da una extracción continua de forma cíclica, disminuyendo el gasto de disolvente y obteniendo altos rendimientos apropiados en la industria metalúrgica.

Nota
Para cada modo de operación, es posible ajustar muchos parámetros, tales como la temperatura del proceso, la temperatura del disolvente, el caudal del disolvente, el caudal de vapor directo y la presión del sistema, lo que permite un alto nivel de experimentación.
Modos de operación
En este apartado, se trata el sistema y el procedimiento por el que se llevan a cabo las operaciones de extracción, tanto para sólido como para líquido, pudiendo ser de dos tipos: extracción en continuo y extracción en discontinuo.
Extracción en continuo
Esta extracción se produce cuando las sustancias que intervienen en la operación se introducen de forma progresiva a lo largo del tiempo y, una vez finalizado el proceso en alguna de sus partes, se retira de forma constante del mismo. Un símil para comprender lo que sería un proceso continuo es la extracción de agua de un pozo con una bomba motorizada: hay un fluir de agua constante del pozo a la superficie.
Extracción en discontinuo
Es un modo de trabajo en el cual se va incorporando al proceso y retirando sustancia de forma completa y, seguidamente, se continúa la marcha de proceso. Un símil que facilita la comprensión es la utilización de un trapo para el secado de un pequeño charco: se le pone el trapo encima y este absorbe el agua, una vez que ya no puede más, se saca, se estruja y se incorpora de nuevo, dando lugar a un proceso discontinuo.
Puede darse en una única etapa o en varias etapas, con la incorporación de nuevas sustancias que intervienen en el proceso, de modo que se mejora el extracto y la sustancia refinada.
3.2. Destilación y rectificación
Cuando se habla de destilación, se hace referencia a una operación básica llevada a cabo para la separación de sustancias, tanto en estado sólido, como líquido y gaseoso, mediante las diferencias de sus puntos de ebullición y sus diferentes volatilidades. Dependiendo de esta tendencia de paso de estado líquido a gas, será llevada a cabo la separación.
Se dispone de varios tipos de destilaciones, desde los procesos más simples, que se han descrito antes, hasta procesos que conllevan una modificación de su naturaleza química. A continuación, se desarrollará cada uno de ellos.
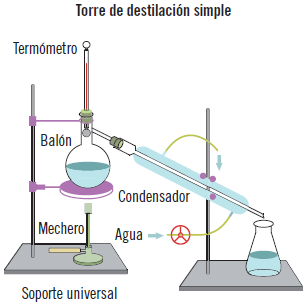
Destilación simple
La destilación simple es el proceso más inmediato de separación de una mezcla, de sus partes no volátiles a las temperaturas en que se opera. En ella, se calienta la muestra hasta el punto donde se evapora la fracción más volátil. Más tarde, este gas se licua con un refrigerador, para obtener la sustancia en su estado original.

Aplicación práctica
Imagine que, tras un accidente de barco, aparece usted en una isla desierta. Su prioridad es conseguir agua, pues no dispone de ninguna fuente de agua dulce, sino solamente de agua salada. Básese en sus conocimientos de separación de mezcla para obtener agua potable.
SOLUCIÓN
Es posible la separación de las sales que contiene el agua de mar mediante evaporación. Al evaporarse, el agua deja sus sales. Para volverla a obtener, solo hay que volver a condensarla. Esta es la parte teórica, a continuación viene la parte técnica. La manera para ejecutarla es con un recipiente cubierto de plástico que se calienta mediante acción del sol, llegando el vapor a este plástico de forma que no se puede escapar y se condensa. Si se coloca otro recipiente donde se vierta este condensado, se dispone de agua potable.
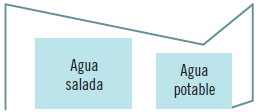
Destilación fraccionada
Para la destilación fraccionada, cuando se dispone de dos sustancias líquidas con sus puntos de ebullición próximos, la destilación simple no produce ninguna separación, por lo que se debe recurrir a una mejora. Esta consiste en la incorporación al montaje anterior de una torre cilíndrica en la cual se colocan una serie de discos, denominada columna de fraccionamiento, donde se establecen equilibrios térmicos y una diferencia de temperaturas más sensible, de modo que solo supera la columna la sustancia de menor punto de ebullición y de la menor regresa al matraz o balón.
Destilación al vacío
En la destilación al vacío, el punto de ebullición de las sustancias en la naturaleza depende de la presión a la que están sometidas. Es sabido que, a medida que aumenta la altura, disminuye la presión y, por consiguiente, la temperatura de ebullición de las sustancias.

Ejemplo
El agua hierve en el Everest a unos 70 ºC, muy por debajo de los 100 ºC en que lo hace en las condiciones normales de un laboratorio.
Destilación azeotrópica
En la destilación arcotrópica se encuentra la mezcla azeotrópica, que es una mezcla en la cual los dos disolventes tienen puntos de ebullición muy próximos, por lo cual no son separables mediante las técnicas anteriores. Estos puntos azeotrópicos se producen en determinas proporciones entre ambos disolventes; hay sustancias que son separables mediante destilación simple o fraccionada, pero cuando sus proporciones alcanzan unos valores fijos, dicha mezcla se comporta como si fuera una única sustancia con un punto de ebullición, donde ambos disolventes se evaporan a la vez, por lo que no son separables.
Para romper esta mezcla azeotrópica, puede hacerse de dos formas:

Ejemplo
En una destilación alcohólica, si se supone una mezcla etanol y agua del 50% y se inicia el proceso, al ser el alcohol más volátil, se evapora antes y se va separando a lo largo del proceso. De este modo, cuando se logre alcanzar el 95% de concentración de etanol, aparece esta forma azeotrópica y todo se evapora a la misma temperatura, por lo que el proceso no se concluye.
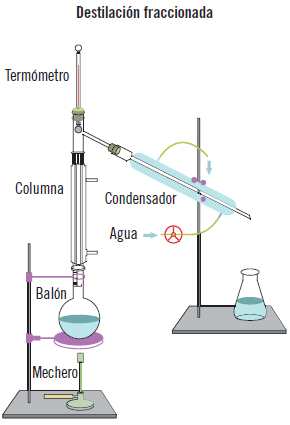
Destilación por arrastre de vapor
La destilación por arrastre de vapor es un tipo de destilación basada en el equilibrio de líquidos inmiscibles. Consiste en la inyección de un flujo de vapor de agua, el cual transfiere su calor a las sustancias a separar y divide las sustancias, formando dos fases distintas, una formada por la incorporación del agua y la otra fase orgánica inicial. De este modo, la sustancia inicialmente no separable por sus bajos puntos de ebullición, ahora se comporta independientemente por la formación de fases inmiscibles.
Destilación reactiva
La destilación reactiva se basa en la incorporación al proceso de destilación de una fase de reacción química, por lo que, al final, se obtiene una sustancia de nueva naturaleza química y totalmente separada del resto. Aunque conlleva una destilación con alguno de los métodos anteriores, es importante mencionarla, ya que esta tecnología forma parte de la producción de muchos derivados del petróleo, siendo una técnica de alta consideración en la industria petrolera.

Ejemplo
Para entender este proceso, se va a suponer un ejemplo genérico de dos sustancias: ácido y alcohol. Para ello, se le incorpora una sustancia denominada catalizador, que favorece la reacción, generando ester y agua, destilándose a continuación y obteniendo la sustancia aprovechable, en este caso el ester.
Ácido + alcohol → Ester + agua
Rectificación
Por su parte, la rectificación es básicamente la destilación de una mezcla de muchos componentes, donde sus puntos de ebullición se mueven en amplios intervalos de temperatura. La rectificación es la forma más importante de desarrollar la destilación y se diferencia de las otras formas en que parte del vapor formado y condensado se devuelve al sistema como líquido, produciendo una corriente denominada reflujo, mejorando la separación.

Nota
En la rectificación, al realizarse condensaciones y vaporizaciones sucesivas, puede conseguirse un sustancial incremento del contenido del componente más volátil en la fase vapor.
Respecto al equipo utilizado para ello, se denomina columna de rectificación y en ella se ponen en contacto en contracorriente una fase líquida descendente y una fase de vapor ascendente. Dicho equipo consta básicamente de una columna cilíndrica con un calderín en su base, en el que hierve continuamente la mezcla a separar, generando el vapor que ascenderá hasta la parte superior de la columna.
El proceso se visualiza como muchas destilaciones o una serie de destilaciones multietapa en una misma operación. Es necesaria una gran torre para que aparezcan las diferencias de temperatura, la máxima abajo en el foco y la mínima en la parte superior. Entre ambas zonas, se sitúan los platos para generar una zona de contacto efectiva.

Recuerde
La destilación es la separación de sustancias mediante evaporación y posterior condensación por la diferencia en sus puntos de ebullición.
A continuación, se mostrará la simplificación de una torre de rectificación. En la parte inferior se sitúa un foco de calor, el cual calienta toda la mezcla multicomponente, produciéndose una distribución térmica asimétrica, la cual avanza de menor a mayor temperatura, de modo que en cada unos de los platos representados en el esquema se produce la destilación de ciertos componentes, según sus temperaturas de ebullición.
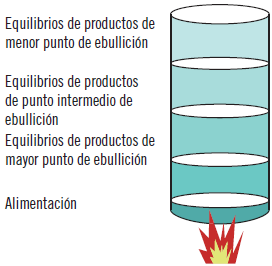
El tamaño de la torre, las volatilidades y la masa de las moléculas producen la distribución asimétrica de las sustancias que componen las muestras a lo largo de la torre, separándose en cada unas de las zonas marcadas con una línea.
Como se observa, la única diferencia con la destilación simple es el uso de la llamada torre de fraccionamiento.

Nota
En ocasiones, esta tecnología es denominada también con el nombre de destilación por fraccionamiento.
No obstante, existen varios tipos de torres de rectificación o fraccionamiento, clasificados según el relleno. Todos los rellenos proporcionan una superficie grande para que las sustancias tengan un contacto más intenso, aunque la función principal del relleno consiste en aumentar la superficie de contacto entre el líquido y el vapor, obteniendo como consecuencia la generación de turbulencias que mejoran en gran medida la eficacia, debido a los anteriores procesos, aunque hay diferencia de temperatura a lo largo de la torre.
La columna puede ser de varios tipos.

Recuerde
Se dispone de varios tipos de destilación: destilación simple, destilación fraccionada, destilación al vacío, destilación azeotrópica,destilación por arrastre de vapor y destilación reactiva.
Modos de operación: continua, discontinua, con reflujo, sin reflujo
Cuando se habla de los modos de operación, se entiende que el sistema por el que se lleva a cabo el proceso de destilación puede ser de varios tipos. La primera clasificación se hace atendiendo al modo de alimentación de material dentro del dispositivo, por el cual puede ser:
En la descripción del proceso anterior, se ha observado cómo hay un equilibrio entre la fase gaseosa producida por un sistema de calentamiento exterior y otra fase producida por la condensación dentro de la torre. Como ya se conoce, en este cambio de estado y dependiendo de las distintas volatilidades de las sustancias de las que se alimenta la torre, se produce la separación. Por lo tanto, en el sistema se dispone de una fracción que queda dentro de la torre y que vuelve al recipiente por la condensación. Si se tienen en cuenta los parámetros mencionados, se dispone de otra nueva clasificación:
3.3. Sedimentación. Decantación. Centrifugación
La sedimentaciónes el proceso por el cual las partículas suspendidas en cualquier tipo de disolución y por el efecto de la fuerza de la gravedad son depositadas en el fondo del recipiente. Esta operación solo es posible cuando el peso de la sustancia a sedimentar es mayor que el del agua y, por supuesto, siempre que no sea soluble, sino que esté suspendida. Este tipo de disolución es conocida como suspensión.
La sedimentación es, en esencia, un fenómeno netamente físico, estando relacionada exclusivamente con las propiedades de precipitación de las partículas en el agua. Cuando se produce sedimentación de una suspensión de partículas, el resultado final será siempre un fluido más claro y una suspensión menos concentrada. Como parámetro físico fundamental que determina la velocidad de precipitación de las partículas en suspensión, se debe a la fricción del agua con las partículas, aunque depende de la densidad del fluido y de la partícula, así como del diámetro de la misma, fundamentalmente.
Dichos parámetros son los que principalmente son modificados para la mejora de la precipitación, los cuales pueden modificar la temperatura, añadiendo algún disolvente que disminuya la densidad o incorporación de floculantes.

Definición
Floculante
Sustancia que se une a otra para precipitar.
La decantación es de nuevo un método de separación basado en métodos físicos, pero, en este caso, de mezclas heterogéneas (aquellas en las que a simple vista se distinguen las dos disoluciones). Es utilizado para la separación de sustancias inmiscibles, llevándose a cabo en un embudo de decantación, donde se coloca la disolución. Por la diferencia de densidad, una fase se sitúa en la parte inferior del embudo y la menos densa se sitúa en la parte superior. Asimismo, este embudo tiene una llave que permite el paso a voluntad, de modo que, cuando ya ha salido toda la fase numerada como 2, se cierra la llave, obteniéndose ambas disoluciones por separado.
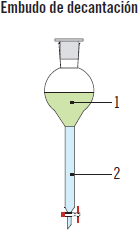
Este técnica es la más simple usada en un laboratorio, siendo el proceso a nivel industrial prácticamente igual, aunque se realiza a gran escala.
Se entiende por centrifugación al proceso por el cual las partículas suspendidas en cualquier tipo de disolución precipitan por acción de una fuerza adicional generada por un movimiento rotatorio. De esta forma, se produce la precipitación de manera forzada a través de esta técnica. En este sentido, se genera una fuerza centrífuga por la rotación del recipiente.

Nota
Se experimenta dicha fuerza centrífuga cuando se toma una curva en un vehículo o se pasa por un resalto, es decir, siempre que se cambia la trayectoria en línea recta.
El dispositivo que genera estas fuerzas es conocido como centrifugadora o centrífuga y básicamente consta de un rotor con unas alas donde se colocan las muestras.

Centrifugadora
La centrifugación es un proceso cotidiano que se lleva a cabo mediante una lavadora automática, la cual produce la separación de un sólido y un líquido (ropa y agua).
La centrifugación puede ser utilizada tanto para aislar partículas como para determinar su peso molecular a través de su velocidad de centrifugación. Además, existen diversos métodos de centrifugación:
La anterior clasificación se debe a la velocidad del rotor de la centrifugadora, pero a su vez se dispone de otro tipo de clasificación atendiendo al medio donde se lleva a cabo:
Importancia y aplicaciones
A continuación, se ha seleccionado una serie de aplicaciones significativas por la importancia de estas operaciones en las empresas del sector.
Sedimentación
En la sedimentación, una de las aplicaciones a destacar dentro de este proceso se produce dentro del tratamiento de las aguas residuales. Aun así, dentro del gran número de procesos se destacan los siguientes:
Ejemplo: eliminación de arenas en el tratamiento de aguas residuales mediante precipitación en piscinas.

Precipitación en piscinas

Recuerde
La sedimentación es, en esencia, un fenómeno netamente físico, estando relacionada exclusivamente con las propiedades de precipitación de las partículas en el agua.

Definición
Velocidad de sedimentación
Cantidad de un compuesto que precipita a lo largo de una hora.
Decantación
La misión de la decantación es eliminar partículas, ya sea por sedimentación o flotación, partículas que, en el caso del tratamiento del agua, proceden de sustancias disueltas que, por la vía de la oxidación, han pasado a insolubles (es el caso del hierro y manganeso disueltos) o por las propias partículas en suspensión existentes en el agua. La mayoría de estas son sedimentables por coagulación-floculación.
Una vez formados los compuestos floculados por la unión de las partículas suspendidas, se debe proceder a la separación de estas mediante decantación en los correspondientes decantadores.

Ejemplo
Una aplicación de la decantación es la eliminación de metales. Este proceso consiste en una decantación con una previa oxidación de sus metales por aireación. Una vez oxidados, precipitan y se continúa con el proceso habitual de decantación.
Centrifugación
Es un proceso con enormes variables y diversas aplicaciones, desde las más cotidianas hasta nuevas formas y modificaciones de alta tecnología, principalmente en la industria alimentaria y en los análisis clínicos. Se pueden destacar las siguientes aplicaciones:

Enriquecimiento de uranio
3.4. Absorción (con o sin reacción química). Desorción o stripping
La absorción es un tipo nuevo de operación unitaria consistente en la separación de una mezcla de sustancias en estado gaseoso, haciéndola pasar por un disolvente donde se formará una disolución de líquido y gas. Básicamente, este proceso se origina por la disolución selectiva de ciertos tipos de gas en determinados disolventes.

Ejemplo
Si se hace fluir una mezcla de aire y amoniaco a través de agua, el aire penetra en el agua y se disuelve en pequeñas porciones, pero el amoniaco desaparece en el agua por su diferente solubilidad acuosa, saliendo por el otro extremo solo aire.
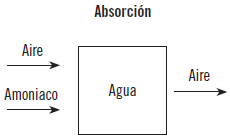
Los procesos de absorción química dependen fundamentalmente de dos parámetros: temperatura y naturaleza de las sustancias que actúan. El agente principal para producir la absorción es el disolvente a utilizar, siendo el más usado y más barato el agua, aunque a veces es necesario utilizar otro.
En ocasiones, se acoplan varios dispositivos de absorción, dando lugar a la absorción multicomponente, con varias etapas de absorción en serie.
La tecnología de absorción consiste en hacer fluir una disolución a través de una torre. En la evolución de esta técnica, ha surgido una implementación, consistente en la incorporación de un relleno en dicha torre para conseguir una mayor superficie de contacto.
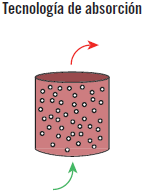
En este esquema, se representa cómo una mezcla gaseosa se introduce a lo largo de una columna de relleno donde queda atrapado unos de sus componentes.
Absorción con reacción química
Cuando dos sustancias interaccionan mediante absorción, puede aparecer un fenómeno de interacción química. En muchos procesos, ocurre, dando lugar a la absorción con reacción química. Normalmente, tanto los reactivos como los productos son solubles en el disolvente donde se da la reacción. Por el contrario, en ciertas reacciones, el producto formado es un compuesto insoluble que precipita en la parte inferior de la torre de absorción.
Un proceso cotidiano en la industria es la formación de dióxido de azufre, producido en la combustión de combustibles fósiles. Estos no pueden ser expulsados a la atmósfera, debido a que son los gases que producen el efecto invernadero, por lo que son absorbidos mediante reacción. El gas de la combustión, con un alto contenido en dióxido de azufre, se pone en contacto con disoluciones de piedra caliza, por lo que se forma sulfito de calcio insoluble, el cual queda en el lecho de la torre.

Sabía que...
El dióxido de azufre es la sustancia generadora de la lluvia ácida.
Desorción o stripping
Cuando se habla de desorción, también conocida por su término anglosajón stripping, se hace referencia al proceso contrario a la absorción, es decir, que se hace fluir una corriente gaseosa a lo largo de una torre, extrayendo el gas uno o varios elementos de la disolución, siendo arrastrados por el gas, que en este caso funciona como extractor.
Un ejemplo de desorción muy utilizado es la potabilización de aguas con alto contenido de compuestos carbonados, proceso al que se denomina burbujeo de aire. Es un proceso utilizado para la potabilización de aguas subterráneas contaminadas con compuestos orgánicos volátiles (COV), principalmente disolventes. El proceso consiste en un flujo en contracorriente de agua y aire a través de un material de relleno, que provee un área de superficie alta para la transferencia de compuestos orgánicos volátiles desde la fase líquida hacia la fase gaseosa, el aire.
En la eliminación de oxígeno con nitrógeno mediante desorción, el nitrógeno es una sustancia que puede interaccionar con el oxígeno. En ocasiones, la alta concentración de oxígeno en ciertas disoluciones puede ser nociva, ya que este puede oxidar compuestos, puede formar radicales libres, etc., por lo que es necesario que su extracción sea llevada a cabo mediante el proceso de desorción. En este caso, se introduce la disolución con exceso de oxígeno y se hace fluir una corriente de aire. El nitrógeno que forma parte de la corriente interacciona con este oxígeno, de modo que es extraído de la disolución acuosa.

Recuerde
La absorción consiste en la separación de una mezcla de sustancias en estado gaseoso haciéndola pasar por un disolvente, donde se formará una disolución de líquido y gas. La desorción es la extracción de uno o varios elementos de la disolución, siendo arrastrados por el gas, que funciona como extractor.
3.5. Cristalización
La cristalización es la técnica operatoria básica, la cual se basa en el proceso físico de cristalización, que consiste la formación de un sólido cristalino (estructura atómica que repite una estructura fija a lo largo de todo el espacio) a partir de un elemento en cualquier estado de agregación, ya sea sólido, líquido o gaseoso.
La cristalización se produce por el proceso físico de sobresaturación. Esta técnica a partir de una solución es un ejemplo de la creación de una nueva fase dentro de una mezcla homogénea. El proceso tiene lugar en dos etapas:
El potencial impulsor de ambas etapas es la sobresaturación, de forma que ni la nucleación ni el crecimiento tendrán lugar en una solución insaturada.

Cristal de cuarzo
Por lo tanto, cuando se habla de cristalización como operación básica, se refiere a aquella técnica en la que se separan sustancias mediante la formación de cristales sólidos y la posterior precipitación de los mismos. No obstante, el tamaño de los cristales puede ser muy variable, lo que produce que se deba acompañar de otra operación complementaria.
Por ello, se dice que la cristalización depende de ciertos parámetros, cuya variación se basa en las distintas técnicas, por lo que se hace necesaria una breve descripción:
AB(sólido) ↔ Bn+ + Am-
Kps = [Bn+]m x[Am-]n
Kps se mantiene constante todo el proceso, mostrando la capacidad para disolver sus iones; si kps es muy elevado, tiene gran capacidad de disolución y viceversa. Para que la reacción se mantenga constante, por ejemplo si hay un exceso de la especie Bn+, el sistema, para mantener dicha constante, tiende a disminuirla cristalizándola, de modo que ese valor numérico no varíe. De igual forma, si disminuye la cantidad de la especie Bn+, el sistema evoluciona, generando esa especie que ha disminuido disolviendo más sólido.
Existen diferentes métodos de cristalización:

Recuerde
La cristalización se produce por el proceso físico de sobresaturación.
A modo de resumen, la cristalización depende de ciertos parámetros, tales como temperatura, concentración iónica y producto de solubilidad, naturaleza del soluto y disolvente.
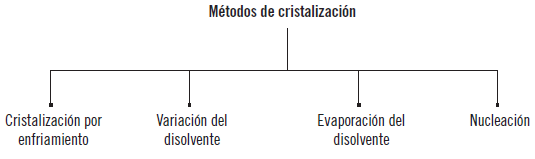
Una forma eficiente de entender los métodos de cristalización es mediante los siguientes ejemplos.
La cristalización es importante como proceso industrial por la enorme cantidad de materiales que son comercializados en forma de cristales. El empleo de productos cristalizados está tan difundido probablemente por la gran pureza de sus formas, por la facilidad para la manipulación del producto químico sólido y por la disminución de la reactividad del producto en este estado. Además, la mayor parte de las aplicaciones industriales (de la operación) incluyen la cristalización a partir de disoluciones. Asimismo, el proceso es el mismo para la cristalización de cualquier producto.

Nota
En términos económicos, la cristalización requiere muchos menos costes para la separación que el resto de procesos de purificación.
Cristalización como parte de la fabricación de azúcar
Se toma una disolución muy pura de sacarosa proveniente del proceso de evaporación. Después, se fuerza la cristalización de la disolución por la adición de cristales perfectos de azúcar, sintetizados en el laboratorio, comenzando de este modo los pasos de nucleación y crecimiento de los cristales. Estos resultan amorfos y de un tamaño poco apropiado, por lo que suele terminar el proceso con una fase de refinado.

Nota
Un buen control sobre el crecimiento del cristal puede economizar los procesos posteriores, llegando al consumidor como un producto de calidad.
Recristalización
Es una operación muy común llevada a cabo dentro del laboratorio, que sirve para purificar distintas sustancias y obtener el mayor grado de pureza posible. El procedimiento consta de una fase de disolución a altas temperaturas, donde solo la sustancia a purificar es disuelta, de modo que se filtra eliminando dichas impurezas. A continuación, se enfría el filtrado, volviendo a cristalizar, pero ya purificado.

Cristalizador de laboratorio
Cristalización como parte del proceso de fabricación de margarinas
Una característica esencial de las margarinas es la presencia de cristales muy pequeños en toda su estructura. Para lograr esto, es necesario realizar un cambio brusco en la temperatura del proceso, de manera que se logre obtener una solidificación con las características mencionadas anteriormente. La cristalización se realiza para obtener pequeños cristales que se dispersan por igual en la fase líquida de la mezcla de grasa mediante nucleación por enfriamiento. Normalmente, los pequeños cristales proporcionan cierta firmeza a la margarina, así como homogeneidad y untabilidad. Además, los cristales son mayores en el área de la superficie total, permitiendo a la fase líquida de la mezcla de grasa adherirse más fácil y eficazmente a la superficie del cristal, reduciendo así el riesgo de destrucción del producto. Por todo ello, este proceso es considerado el más importante en la producción de margarinas, el cual es realizado en un tubo perfector.

Cristalizadora industrial para la producción de margarina
El tubo perfector es un dispositivo que permite el intercambio de energía, de modo que se formen dichos cristales por enfriamiento, pero a la vez no adquiera una densidad muy alta. Para ello, dispone de unas cuchillas para batir la margarina durante todo el proceso, obteniéndose una margarina uniforme.
3.6. Humidificación. Secado. Liofilización
Este apartado se ocupa de aquellas operaciones básicas que suponen una variación en el porcentaje de agua de las sustancias, siendo considerada una operación básica que cobra gran importancia en la industria alimentaria. Se trata de hidrataciones y deshidrataciones llevadas a cabo del mismo modo.
Humidificación
Es una operación básica producida por el intercambio de energías en forma de calor junto a una transferencia de materia acuosa. En este caso, van unidas las dos variables de control de los procesos:
Esta operación tiene por objeto modificar las condiciones de humedad de la sustancia.

Nota
Se puede aplicar a cualquier sistema gas/líquido, aunque la aplicación más extendida es al sistema aire/agua.
Este fenómeno conduce a diferentes aplicaciones, como son la deshumidificación, el enfriamiento del gas y el enfriamiento del líquido, además de permitir la medición del contenido de vapor en el gas. Si se toma el ejemplo más simple, agua líquida y aire en fase de gas, y se hace fluir uno sobre otro, se observa que aparece aire húmedo y el agua ha perdido parte de su masa y disminuido la temperatura de ambos. En la industria, se usa para la refrigeración, la humidificación y la deshumidificación o secado.
Se puede resumir el proceso de humidificación en los siguientes pasos:
Por otro lado, se dispone de varias tecnologías para la humidificación, que se describen a continuación.
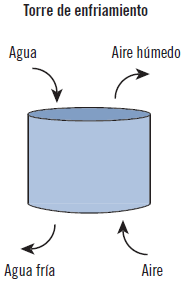
Torre de enfriamiento
Es la de uso más extendido por su amplia utilización en distintos procesos. Es una torre de relleno muy similar a las anteriores donde se rocía en forma de lluvia el agua desde la parte superior de la torre. El aire asciende a través del relleno de la torre, de modo que se produce una refrigeración efectiva y económica.
Humidificación de alimentos
Para la conservación de los alimentos, hay dos factores muy importantes que son la temperatura y la humedad.
El sistema de humidificación de alimentos consiste en la aplicación de una fina capa de humedad, constituida por microgotas que cubren la superficie de los alimentos.

Humidificador de alimentos
Deshumidificación o secado
La deshumidificación es una operación que consiste en reducir la cantidad de agua presente en una sustancia mediante una vaporización o condensación del vapor de agua. Se puede llevar a cabo mediante un contacto directo entre la fuente de calor o de forma indirecta.
Las condiciones del secado dependen de tres parámetros:
Además, los dispositivos para producir secados pueden ser los siguientes:
En lo que se refiere a sus aplicaciones industriales, cabe señalar las que se describen a continuación.
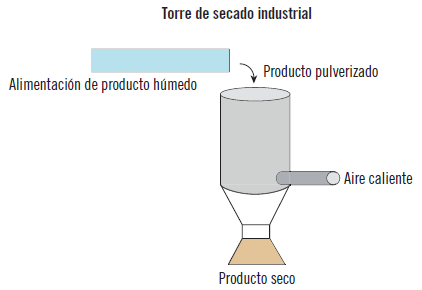
Torre de secado para papillas
Es la forma más eficiente de secar materiales orgánicos e inorgánicos, catalizadores, cerámicas, metales pulverizados, pigmentos, tinturas y otros similares. Produce secados a altas temperaturas con un chorro de aire caliente. Además, posee una alta capacidad de evaporación, dependiendo del perfil de temperatura del aire de entrada/salida y de la composición de la alimentación. El proceso comienza con la pulverización mediante boquillas ubicadas en la parte superior de la torre, dejándose caer en forma de lluvia. Por otra parte, desde la parte inferior sale un flujo de aire. La sustancia a secar, a medida que desciende por efecto de la gravedad y en su contacto con el aire a mayor temperatura, va cediéndole su agua, de modo que llega al fondo de la torre donde hay un silo para recoger su producto.
Secado de alimentos
Es un método para conservar alimentos, mediante la eliminación de agua, para eliminar los microorganismos que producen la putrefacción. Es un proceso muy antiguo, para la conservación de frutas, pescados y carnes. El proceso se lleva mediante corriente de aire en una bandeja o en túnel de secado.

Recuerde
La deshumidificación es una operación que consiste en reducir la cantidad de agua presente en una sustancia, mediante una vaporización o condensación del vapor de agua.
Liofilización
Es la operación básica, basada en la extracción de agua, mediante dos procesos:
En este caso, se congela la sustancia y se introduce en una cámara de vacío para producir la separación del agua, mediante sublimación, es decir, el agua se evapora y queda el resto de la mezcla. En ocasiones, la extracción no es completa, por lo que se vuelve a repetir el proceso.

Nota
Los factores que influyen en el proceso de liofilización son los mismos que en la congelación, además de los propios de la sublimación al vacío.
Respecto a las aplicaciones de la liofilización, algunas de las más importantes son:

Liofilización en el campo alimentario

Recuerde
La liofilización es la operación básica, basada en la extracción de agua, mediante dos procesos: congelación y sublimación.

Aplicación práctica
Usted va a realizar un viaje en barco de tres meses y, una vez que está en el barco, a los pocos días de zarpar, ve cómo el refrigerador deja de funcionar, por lo que debe buscar un método para la conservación de la fruta los más rápido posible conservando la mayor parte de sus nutrientes. ¿Qué método de conservación usaría? ¿Cuáles son las ventajas que ofrece este método?
SOLUCIÓN
De entre los métodos de conservación que se conocen, el más accesible es el secado de la fruta. Algunas frutas dan mejor resultado que otras. En el plátano, la manzana, los albaricoques etc., es posible reducir el contenido de agua, llegando a una quinta parte de su peso y, de este modo:
3.7. Filtrado y ósmosis inversa
El filtrado es una técnica que puede resultar realmente simple, pero es que ha sufrido un proceso de transformación a lo largo de muchos siglos. Una de las principales filtraciones es la eliminación de arena del agua destinada al consumo humano, pero, desde esta, se ha desarrollado una verdadera teoría científica bastante compleja.
La principal limitación reside en el hecho de las características de la mezcla en dos estados de agregación fijos (sólido y líquido), por lo que se deben tener en cuenta todas la interacciones que pueden surgir.
Si se establecen los principios básicos, se puede determinar como parámetro básico el fluir del caudal, a través de la resistencia u oposición del filtro.
Para hacer fluir cualquier sustancia, es necesaria una fuerza que lo produzca, denominada fuerza impulsora. Esta suele ser la fuerza de la gravedad, aunque, en algunos casos, es necesario un suplemento (bombas de presión o de centrifugación, etc.).
La velocidad de fluido depende de los siguientes parámetros:
Todas las sustancias se caracterizan por ser de escasa actividad química, baja densidad y alta superficie, de modo que todas las propiedades aumentan la velocidad de flujo. Todo se dispone en una combinación de los siguientes aparatos de laboratorio: trípode, embudo y filtro.
La velocidad de filtración es directamente proporcional a la presión aplicada y al área, mientras que es inversamente proporcional a la viscosidad de la corriente de fluido, a la cantidad de torta formada y al tamaño de las partículas que lo forman.

Nota
La nanofiltración consiste en una técnica de filtrado en la que se usa un filtro de un tamaño, en sus conductos, del orden 10-9 m, ayudado por una fuerza adicional.
Ósmosis inversa
La ósmosis inversa es el proceso por el cual se establece una relación de equilibrio entre dos fases fluidas, la cuales contienen o pueden contener un determinado soluto.
La ósmosis inversa produce un equilibrio entre ambas fases, de modo que se produce un trasvase de sólido.
Este proceso se puede realizar debido a la colocación de una membrana semipermeable (solo se permite el paso de fluidos y no solutos). Por lo tanto, cuando se ponen en contacto dos fases con una cantidad de soluto distinto, se inicia el proceso de equilibrio, pasando solamente disolvente de una a otra, a través de la membrana. Al final, se obtiene la deseada situación de equilibrio y la extracción buscada. Aparece un proceso ligado a este fenómeno, la presión osmótica, es decir, la presión ejercida por la mayor altura de una de las mezclas unidas por la membrana.
Ejemplo de desalinización de aguas
Se trata de llevar a cabo el proceso de presiones, en sentido contrario. Las sales se extraen cuando dos fases se unen a través de una membrana semipermeable, se ejerce presión en uno de los depósitos, pasando únicamente agua de un lado a otro de la membrana y quedando las sales de salmuera en el lado donde se aplica dicha presión.
3.8. Molienda. Tamizado
En este apartado, se tratarán las dos operaciones unitarias cuyo objetivo es la adecuación del tamaño del material, la primera modificando mecánicamente el tamaño de grano y la segunda por selección de la materia de tamaño apropiado.
Molienda
La técnica de molienda consiste en la disminución del tamaño de grano y en la trituración de sustancias para que sean utilizados en otros procesos.

Sabía que...
Desde hace 4 milenios, la molienda del trigo formaba parte de las tareas del ama de casa, donde apareció el molino manual rotatorio, haciendo girar una piedra superior sobre otra inferior por medio de un palo. Este representa unos de los ejemplos más antiguos de utilización de esta técnica, también usado independientemente por las culturas prehispánicas en la zona del Golfo de Méjico, tanto para moler cereal de trigo como de maíz.

Molcajete mexicano
Tamizado
Es una técnica consistente en la separación de dos sustancias por la diferencia en el tamaño de su grano. Al hacer pasar esta mezcla por un filtro de un tamaño intermedio a las dos sustancias, unas atraviesan la malla y otras se quedan, por lo que al final se obtienen las componentes de la mezcla por separado.
Es un método muy sencillo utilizado generalmente en mezclas de sólidos heterogéneos.
Lógicamente, por su proceso, este método solo es aplicable a fases que se presentan en estado sólido. Se utilizan tamices de tamaño de malla variable, de metal o plástico.
Este tamiz de tejido no es más que una serie de hilos colocados a lo ancho y en sentido vertical, formando una superficie dotada de perforaciones uniformes.
3.9. Agitación y mezcla
Es un método cuyo fin no es más que buscar el contacto más íntimo y, de esta forma, favorecer todos los procesos de equilibrio que conducen a la consecución de algunas de las técnicas mostradas.
Cuando se habla de agitación, se refiere a forzar un fluido por medios mecánicos para que adquiera un movimiento circulatorio y caótico en el interior de un recipiente. Los objetivos de la agitación pueden ser:
Generalmente, el equipo consiste en un recipiente cilíndrico, para favorecer el movimiento circulatorio, con un eje accionado por un motor.
El agitador crea un flujo dentro del dispositivo, dando lugar a que el líquido circule por todo el recipiente y vuelva de vez en cuando al agitador.

Nota
Estos dispositivos tienen por objeto la obtención del estado de mezcla. En química, se refiere esa mezcla como la unión de diversos elementos que no son separables por métodos ajenos a un laboratorio.

Aplicación práctica
Se encuentra en un laboratorio con una mezcla de tres sustancias: sulfato de cobre (sal soluble), arena (insoluble) y virutas de hierro. ¿Cómo debería usted actuar para separar las tres sustancias?
SOLUCIÓN
Primero, se toma la mezcla, se le incorpora agua y se agita para que aquellas sustancias solubles se disuelvan. El sulfato de cobre se filtra y, por un lado, se obtiene una disolución de la sal, que mediante cristalización será recuperada.
A continuación, en el filtro, se retienen la arena y las virutas. Se puede usar un imán para separar ambos componentes de la mezcla.
3.10. Transporte de fluidos
Dentro de la industria, es muy importante llevar de un lado a otro las distintas sustancias y,en este caso, para el fluido (gases o líquidos), cobra una especial importancia por la dificultad que implica. Esto es producido por dos dispositivos:
Las bombas y ventiladores convierten la energía mecánica procedente de cualquier fuente en una presión o generan una velocidad, que es adquirida por el fluido.
La eficiencia del transporte con una bomba depende de los conductos que llevan el fluido y de la potencia que es capaz de trasmitir la misma.

Importante
Las bombas son de gran importancia en el transporte de fluidos, debido a su capacidad de producir vacío, con lo cual se puede empujar el fluido hacia donde se desee transportar.
Cuando se transportan fluidos, es necesario suministrar energía para vencer las pérdidas por rozamiento. Para elegir una bomba adecuada, se deben considerar las siguientes variables:
Se pueden distinguir, en general, dos tipos de bombas:

Nota
Las bombas de vacío son dispositivos muy utilizados en la industria para el trasporte. La bomba crea una zona de baja presión y el aire fluye hacia esa zona para compensar y restablecer equilibrio. El aire arrastrado lleva consigo el fluido que esté presente en el medio.
3.11. Transporte de sólidos
Dentro de la industria, se usan varios métodos para el transporte, pero de todos ellos el neumático proporciona mejores resultados en el transporte de productos secos, finos y a granel.
Para la elección o diseño de un correcto sistema de transporte, es necesario tener en cuenta los siguientes parámetros:
El transporte se diseña en función de la trayectoria que se lleva a cabo:
En este capítulo, se han visto los distintos procesos realizados en la industria química, que se basan en intercambios de masa y energía entre los distintos sistemas que interaccionan.
Las leyes que controlan dichos procesos y sus balances se basan en unos principios fundamentales que controlan los procesos universales, estos son los principios de Conservación de la Masa y de la Energía. A partir de ellos, se han descrito todos los procesos de separación de sustancias, en todos los estados posibles, mediante las técnicas habituales de laboratorio, comenzando por extracciones y destilaciones, con ejemplos de los procesos más habituales, hasta llegar los procesos de cristalización.
A continuación de los métodos generales, aparecen unos procesos específicos de separación de sustancias relevantes en la naturaleza, habiéndose hecho especial hincapié a la extracción de agua, en los apartados de secado y deshumidificación.
Se ha finalizado el capítulo comprendiendo los fenómenos previos y finales del transporte de toda sustancia.

1. Una operación básica es:
2. El concepto de continuidad en una operación química se refiere...
3. Enumere cuatro parámetros de los que dependa el proceso de extracción.
4. De las siguientes frases, indique cuál es verdadera o falsa.
a. La lixiviación es una operación de extracción sólido-sólido.
b. Solo se puede hacer un uso de la destilación cuando los disolventes tienen distintos puntos de ebullición.
c. Un proceso muy eficiente para la eliminación de sustancias muy disueltas es la floculación.
d. La cristalización se produce por la sobresaturación de una disolución por cualquier método.
e. La evaporación del disolvente es una técnica de formación de núcleos para dar lugar a la cristalización.
5. Complete la siguiente oración.
La ___________ de plasma sanguíneo es el proceso que se desarrolló comercialmente en la ___________, por sus enormes ventajas, debido a que se conservan perfectamente todas las ___________ del plasma y se evita su ___________, con el correspondiente deterioro de su ___________.
6. Complete el siguiente esquema.
7. ¿Cuáles son los usos más importantes de la operación de centrifugación?
8. Se dispone de una mezcla de aceite y agua, ¿qué método utilizaría para la separación de ambas sustancias?
9. Complete la siguiente tabla.
| Tipo de enlace | Conducen la electricidad | Estado en la naturaleza a temperatura ambiente |
|---|---|---|
| Covalente | ||
| Metálico | ||
| Iónico |
10. ¿Qué métodos de cristalización existen?