CAPÍTULO
2

La potencia motriz del fuego
Es necesario que también haya frío; de lo contrario, el calor sería inútil.1
SADI CARNOT
Es un muchacho extremadamente gentil, se comporta bien y es algo tímido […] Su seguridad no debe minarse.2
SADI CARNOT, descrito por un amigo
Todavía en la veintena, de complexión media y «constitución delicada», Sadi Carnot era reservado e introspectivo y llevaba una vida solitaria. Pocos eran los alumnos del Conservatorio Nacional de Artes y Oficios de París que, a principios de la década de 1820, le hacían demasiado caso. Un retrato que se ha conservado de él nos muestra a alguien cultivado, pensativo y, en cierto modo, de apariencia frágil.
Sadi Carnot nació el 1 de junio de 1796 en una estancia del palacio Petit Luxembourg, en París.3 Su padre, Lazare, fue un brillante matemático e ingeniero4 que, de joven, había publicado un artículo en el que proponía formas de mejorar el famoso globo aerostático que los hermanos Montgolfier presentaron en 1783. Los otros ensayos científicos de Lazare incluían estudios sobre los principios que apuntalaban el funcionamiento de máquinas como los molinos de agua. Era también admirador de un poeta persa del siglo XIII, Saadi de Shiraz, de ahí el inusual nombre de pila que escogió para su hijo.
En 1789, cuando estalló la Revolución francesa, Lazare se metió en política; dos años después fue elegido diputado de la cuasi democrática Asamblea Legislativa del país y se hizo un nombre gracias a su efectiva reorganización del Ejército Revolucionario Francés. Lazare también fue un tipo con suerte, pues sobrevivió al Terror, a diferencia de muchos otros revolucionarios franceses destacados. Cuando Sadi nació, en 1796, su padre era uno de los cinco miembros del Directorio que gobernaba el país, de manera que el niño creció en el epicentro de la mayor agitación política e intelectual de la Europa del siglo XVIII.
El propio Lazare Carnot educó a Sadi cuando era pequeño, pero cuando sus aptitudes para la ciencia se hicieron patentes, lo mandó al prestigioso centro francés de educación científica superior, la Escuela Politécnica de París.5 Igual que el Conservatorio Nacional de Artes y Oficios,6 al cual Sadi Carnot terminaría asistiendo más adelante, la Escuela Politécnica se había fundado en 1794 dentro del compromiso del gobierno revolucionario francés con la educación pública. (Lazare Carnot fue uno de sus fundadores.) Los miembros de la escuela encargados de la selección de los alumnos viajaban por toda Francia con la misión de encontrar a los candidatos con más talento del país, al margen de los recursos de sus familias. La estrategia funcionaba hasta cierto punto, pero en general, los alumnos procedían principalmente de las clases pudientes. Los exámenes de acceso eran exigentes, y la mejor forma de superarlos era recibiendo formación de un lycée parisino de élite o clases particulares, como era el caso de Carnot. Se matriculó en noviembre de 1812; a los dieciséis años era el tercer aspirante más joven del curso, y quedó en vigesimocuarto lugar en un grupo de 184 estudiantes.
En la Politécnica, Carnot recibió dos años de formación ejemplar en los últimos descubrimientos en los campos de las matemáticas y de la física, y se graduó en octubre de 1814. Estaba destinado a formar parte de las fuerzas de ingeniería dentro del ejército francés cuando la historia intervino. El 18 de junio de 1815, las fuerzas británicas, prusianas y otros aliados europeos derrotaron a Napoleón en Waterloo y lo desterraron a la remota isla de Santa Helena, en el Atlántico medio. Más de un millón de soldados extranjeros, el llamado Ejército de la Séptima Coalición, ocuparían Francia y coronarían a un nuevo rey, Luis XVIII, hermano de Luis XVI, quien había sido decapitado durante la Revolución. Estos acontecimientos dejaron a la familia Carnot en una situación desastrosa, en gran parte porque Napoleón había nombrado a Lazare Carnot ministro del Interior poco antes de su derrota. Su cercanía con Napoleón hizo que el régimen francés posterior a Waterloo desconfiara de él y, por tanto, lo exiliaron a la ciudad de Magdeburgo, en Alemania. Sadi Carnot se quedó en París, donde lo trataron como a un paria. Durante el gobierno de Napoleón, los soldados franceses de alto rango buscaban a Sadi y lo lisonjeaban por su apellido; ahora, sus nuevos superiores militares lo marginaban y lo destinaban a regiones remotas de Francia. Debió de sentir un gran alivio cuando, en 1819, obtuvo un puesto como teniente en París. Aunque le bajaron el sueldo a la mitad y debía realizar algunos ejercicios de entrenamiento militar ocasionales, lo dejaron ir a su aire.
Carnot dedicaba su tiempo libre a cultivar su interés por la ciencia y la tecnología. Visitó las fábricas de las zonas industriales emergentes de París y enriqueció su formación científica previa asistiendo a conferencias en el Conservatorio Nacional de Artes y Oficios, donde Jean-Baptiste Say daba clases. Ubicado en el este de París, el gobierno revolucionario había establecido el Conservatorio en lo que antes fue un monasterio y compartía con la Escuela Politécnica la misión de mejorar la educación pública. El gobierno borbónico, ya reinstaurado, siguió financiándolo, pero dada su asociación con los regímenes anteriores, sospechaba de muchos de sus profesores y alumnos de estar tramando una rebelión secreta y lo llenó de espías.
A pesar de ello, el Conservatorio era un lugar con un rico espíritu de investigación, y en él Carnot conoció al profesor de Química, Nicolas Clément, quien le enseñó todo lo que se sabía acerca de la temperatura y el calor.
De esos dos conceptos, el de temperatura era el más sencillo. Para hacernos una idea intuitiva acorde con la visión de principios del siglo XIX, pensemos en la temperatura como la medida de lo caliente que algo nos parece. Imaginemos, por ejemplo, una olla grande y una sartén pequeña. Las dos están llenas de agua del mismo grifo. Si metemos un dedo en cualquiera de ellas, la sensación será similar. Si metemos un termómetro en cualquiera de ellas, nos dará la misma cifra.
El calor es mucho más difícil de entender. Si colocamos los dos mismos recipientes sobre el fuego, la temperatura del agua que contienen aumentará a medida que el gas vaya liberando «calor» al quemarse. Pero para alcanzar el mismo aumento de temperatura, tendremos que mantener el recipiente más grande al fuego durante mucho más rato que el pequeño. Estas observaciones implican que el calor tiene el efecto de aumentar la temperatura de una sustancia más o menos en función de la cantidad de dicha sustancia. Pero ¿qué es el calor? ¿Qué es eso que emana del gas que quemamos y que calienta las cosas?
En la época de Clément y Carnot, la mayoría de los científicos creían que el calor era una materia invisible llamada calórico que estaba compuesta de unas partículas diminutas e ingrávidas que liberaban las sustancias al arder. Se suponía que estas sustancias calóricas se repelían entre ellas, y por eso el calor tendía a ir de frío a caliente a medida que iba igualando las diferencias de temperatura. Al empujarse las unas a las otras, las partículas de calórico rezumaban de los microscópicos poros que se creían presentes en todos los materiales, dispersándose a través de ellos y calentándolos por el camino. Cuanto mayor fuera el volumen de la sustancia, más calórico haría falta para provocar el aumento de temperatura deseado. Pero el calórico no solo calentaba las cosas, también podía hacer que se derritieran o hirvieran. Muchos científicos consideraban que el calórico era un elemento gaseoso como el oxígeno, que podía fluir de un lado a otro. Y con el calórico ocurría lo mismo que con los elementos como el oxígeno: no se podía ni crear ni destruir.
Sin embargo, a principios del siglo XIX, muchos científicos se dieron cuenta de los puntos débiles de la teoría calórica. Uno de ellos fue Benjamin Thompson, un científico estadounidense que había emigrado a Múnich y que trabajaba como ayudante de campo del gobernador de Bavaria. Una de sus funciones era supervisar el arsenal nacional, y observó que cuando se abría el hueco de las ánimas de los cañones con una herramienta que se parecía a una broca gigantesca, la fricción generaba una enorme cantidad de calor. Para investigarlo, Thomson sumergió el ánima de un cañón en agua mientras lo taladraban. Dos horas y media después, se había generado tanto calor que el agua empezó a hervir.
En un artículo enviado al organismo científico más importante de Gran Bretaña, la Real Sociedad de Londres para el Avance de la Ciencia Natural, Thompson afirmaba que, a pesar de que la teoría calórica explicaba por qué al quemar se liberaba calor, no alcanzaba a justificar por qué se liberaba a partir de la fricción. En el primer proceso, era plausible que las partículas calóricas que estaban atrapadas escaparan a medida que ardía el combustible; cuando el combustible se terminaba, dejaba de liberarse calórico. En cambio, la fricción parecía ser una fuente inagotable de calor. Mientras el esfuerzo mecánico se dedicase a frotar un objeto contra otro, surgiría calor. En otras palabras, la fricción parecía crear calor, no liberarlo. Aquello contradecía la afirmación de la teoría calórica según la cual el calor no se podía ni crear ni destruir. (Thompson, crítico acérrimo de la teoría calórica, se casó con Marie-Anne Lavoisier, viuda de uno de los fundadores de la teoría, el famoso químico francés Antoine Lavoisier, que había sido ejecutado durante el Terror. El matrimonio de Thompson y madame Lavoisier fue breve.)7
Además de los puntos fuertes y débiles de la teoría calórica, Carnot aprendió acerca de la aportación que el propio Clément había hecho al estudio del calor: había diseñado una forma objetiva de cuantificarlo. Antes de Clément, y a pesar de que hiciera más de un siglo que se venían construyendo máquinas de vapor, no existía una unidad de medida universal para las cantidades de calor. A los ingenieros de minas de Cornualles se les había ocurrido el concepto de la «capacidad» de un motor, la cual equivalía al peso del agua en libras que se elevaba una altura de un pie cuando se quemaba una fanega de carbón, o unos 38 kg, en la caldera. Pero no habían pensado en cuantificar el calor que surgía del carbón al quemarlo. También se sabía, por ejemplo, que se tardaba más en hervir un litro de agua que un litro de alcohol, pero no existía convención numérica alguna para comparar las distintas cantidades de calor. Y ese fue precisamente el método que diseñó Clément.
Todo esto lo sabemos gracias a un relato anónimo de las clases de Clément8 que se ha conservado. En él aparecen estas históricas palabras: «El señor Clément imagina una unidad de calor a la que llama la “caloría”. Una caloría es la cantidad de calor necesaria para aumentar la temperatura de un kilogramo de agua en un grado centígrado». Ese sigue siendo el sentido de caloría cuando se emplea para medir el contenido energético de la comida. Por ejemplo, una bolsa de patatas fritas de 100 g que contiene unas 500 calorías, según la definición de Clément, liberará el suficiente calor como para aumentar la temperatura de 500 kg de agua en 1º C. (Algunas décadas después, los científicos redefinieron la caloría con el significado de cantidad de calor necesaria para elevar la temperatura de un gramo de agua, en lugar de un kilogramo de agua, en 1º C, lo que significa que una de las calorías de Clément equivale a mil calorías de las de hoy.)
A Carnot también lo influyeron los artículos científicos de su padre, Lazare, escritos durante la década anterior a la Revolución. En uno de ellos, titulado «Ensayo sobre las máquinas en general», Lazare había analizado matemáticamente el comportamiento de los molinos de agua.
Más concretamente, Lazare imaginó el molino ideal,9 en el que toda la «potencia de empuje» del agua se convierte en el movimiento rotativo de la rueda, sin que se desperdicie un ápice de energía. En su molino, el agua se ralentiza de manera paulatina a medida que hace girar la rueda, transfiriendo toda su velocidad de flujo al movimiento de rotación de esta. Lazare observó que los molinos reales se quedaban muy cortos en comparación con esta situación ideal, pero apenas dijo nada sobre cómo ponerle remedio, y se centró en utilizar las matemáticas para describir los aspectos de la física que explican la potencia del agua. A nadie le sorprendió que los fabricantes de molinos prestaran muy poca atención al razonamiento abstracto de Lazare, pero su hijo se serviría de su enfoque para dar pie a grandes consecuencias científicas.
En 1821, Carnot se desplazó a Magdeburgo para pasar unas semanas con su padre y su hermano pequeño en el exilio. El momento le fue propicio. La primera máquina de vapor de la ciudad la había instalado tres años antes un ingeniero inglés expatriado,10 una de tantas construidas por hombres como él en la Europa continental en aquella época. No es descabellado especular que Lazare y Sadi fueran a ver la máquina de vapor y fueran testigos de por qué los británicos estaban a la cabeza en tecnología a base de vapor. En cualquier caso, cuando Sadi Carnot regresó a París, se puso a trabajar inmediatamente en un texto seminal. Cuando lo terminó en 1824, lo tituló Reflexiones sobre la potencia motriz del fuego y sobre las máquinas hechas para desarrollar dicha potencia. Con «potencia motriz», Carnot se refería a la cantidad de trabajo útil, como el bombeo de agua para sacarla del pozo de una mina o proporcionar energía a un barco, que se puede obtener del calor que se crea en el «fuego» o en la caldera de una máquina de vapor.
El texto de Carnot no se parece en nada a un artículo científico actual. Su deseo de que lo pudieran «entender personas ocupadas con otros estudios» —es decir, todo aquel que no fuera científico— queda demostrado en su exposición lúcida y libre de términos técnicos. Antes de explicar datos científicos, Carnot trata de convencer al lector de que la ciencia importa. Hace hincapié en los beneficios de la forma en que las máquinas de vapor utilizan el calor para llevar a cabo tareas que hasta entonces habían exigido fuerza animal, viento o agua en movimiento al escribir: «Parecen destinadas a producir una gran revolución en el mundo civilizado». Incluso defiende el potencial utópico de esta tecnología: «La navegación a vapor acerca a las naciones más distantes. Tiende a unir a las naciones de la Tierra como habitantes de un único país». Y para demostrar qué es capaz de lograr la máquina de vapor, Carnot apunta hacia el otro lado del canal de la Mancha: «Arrebatarle hoy a Inglaterra sus máquinas de vapor […] significaría destruir todo de lo que su prosperidad depende […] aniquilar esa potencia colosal».
Carnot termina su introducción con una declaración de intenciones: «Al margen del trabajo de todo tipo ejercido por las máquinas de vapor […] su teoría se comprende muy poco, y los intentos de mejorarlas todavía siguen guiándose por el azar».
Así, para Carnot, deducir la teoría que hay detrás de las máquinas de vapor no era un ejercicio académico. Consideraba que, al hacerlo, se obtendría una forma de mejorar la eficiencia del combustible, lo que a su vez reduciría los costes soportados por los empresarios industriales de su país y los ayudaría a ponerse al nivel de sus homólogos británicos. Para Carnot, la pregunta fundamental era: ¿cómo se obtiene la mayor potencia motriz posible a partir de una máquina de vapor?
Entonces, Carnot lleva más lejos la idea de la capacidad de una máquina de vapor. En lugar de preguntar cuánto carbón debe consumirse para elevar un peso conocido una distancia concreta, Carnot plantea cuánto calor debe salir de la caldera para lograrlo. O, dicho de otra forma: suponiendo que salen 100 calorías de calor de una caldera, ¿cuál es la altura máxima a la que esta puede elevar un peso de 1 kg? (Para hacerlo más sencillo, pensemos que una unidad de «potencia motriz» es la cantidad que elevará un peso de 1 kg una altura de 1 m.)
Para responder esta pregunta, Carnot se fija en una máquina de vapor típica de principios del siglo XIX que funciona según lo diseñado por James Watt. Al científico francés le interesaban dos aspectos especialmente.11
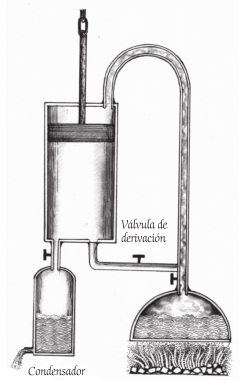
Imagen impresionista de los aspectos clave de la máquina de vapor de Watt
Primero, Watt se había dado cuenta de que el vapor caliente ejerce una gran presión, más incluso que el peso de la atmósfera. Para sacarle partido, ideó su diseño de forma que el vapor que se expandía desde la caldera empujara un pistón. (En el diagrama, el vapor empuja el pistón hacia abajo.)
Luego, Watt comprendió que para que la máquina siguiera funcionando, el pistón debía retomar su posición inicial en la parte superior del cilindro, lo que depende de que el vapor que lo ha empujado hacia abajo se enfríe y se condense en forma de agua para que deje de ejercer presión sobre el pistón. Entonces, una fracción de la fuerza motriz generada en el movimiento hacia abajo se emplea para empujar el pistón de nuevo hacia arriba.
Watt logró que todo esto fuera posible con un dispositivo llamado condensador que se mantiene frío gracias a un chorro de agua. Cuando el pistón se sitúa cerca del fondo del cilindro, la válvula de derivación y la válvula de entrada del condensador se abren. El vapor que se encuentra por encima del pistón fluye a través de estas válvulas y se convierte en agua en el condensador, de forma que deja de ejercer presión sobre el pistón.
En su tratado, Carnot ignora cómo funcionan los componentes de la máquina de vapor y decide centrarse en el flujo del calor a través de todo el circuito. Siguiendo la teoría calórica, afirma que una cantidad de fluido calórico indestructible, liberado a partir de la quema de carbón en la caldera, se «incorpora» al vapor, elevando así su temperatura y su presión para que pueda empujar el pistón hacia abajo. Entonces, en el condensador, el calórico se separa del vapor, el cual se enfría y se vuelve líquido. A medida que la presión del vapor disminuye, el pistón regresa a su posición.
La conclusión a la que llega Carnot es que una cantidad fija de calórico fluye desde la caldera caliente hasta el condensador frío, y ese flujo genera la potencia motriz de la máquina. Lo equipara al flujo del agua: igual que no se pierde agua mientras su flujo hacia abajo mueve el molino, aquí tampoco se pierde calor mientras su flujo «enfriador» mueve la máquina de vapor.
Carnot se equivocaba al creer en la teoría calórica, pero ese convencimiento lo condujo a su primer avance. Un cuerpo de agua, por muy vasto que sea, no generará potencia motriz a menos que pueda fluir hacia abajo. De igual modo, incluso una cantidad ingente de calor no generará potencia motriz si no se da una diferencia de temperatura desde la que pueda «fluir hacia abajo». Una máquina de vapor colocada en el interior de una caldera no funcionará por mucho calor que haya, porque no tiene forma de enfriar el vapor y hacerlo líquido para que el pistón reciba el empuje que lo lleve de vuelta hacia la parte superior del cilindro. Carnot escribe:
«La generación de calor por sí sola no basta para dar lugar a la potencia de impulso: es necesario que haya también frío; sin él, el calor resultaría inútil.»
Esta frase marca el primer paso de la historia de la termodinámica.
A continuación, Carnot aborda una cuestión que irritaba a los ingenieros de su época: ¿es el vapor la sustancia más efectiva en las máquinas que extraen potencia motriz del calor? Después de todo, cualquier gas, y no solo el vapor, se expande si lo calentamos, aumentando de esta manera la presión que ejerce, lo que significa que cualquier gas puede empujar un pistón. Así, ¿podría una máquina que funcionara, por ejemplo, a partir de aire atmosférico o de vapor de alcohol generar más potencia motriz a partir de una cantidad concreta de flujo de calor que una máquina de vapor? ¿Podría dicha máquina emplear el calor que surge de quemar 1 kg de carbón para elevar un peso concreto hasta una altura superior a la que sería capaz de alcanzar una máquina de vapor?
En su afán por responder esta pregunta, Carnot ignora todos los detalles relacionados con la ingeniería que entran en juego en una máquina y, en cambio, se sirve de una estrategia que aprendió de su padre y parte de máquinas imaginarias para armar su planteamiento.
Carnot le pide al lector que se imagine una máquina de vapor ideal, es decir, una que pueda generar la máxima potencia motriz posible —que pueda elevar un peso concreto hasta la mayor altura posible— a partir de un flujo de calor concreto que se desplace desde un punto caliente hasta otro frío. (Para simplificar, me referiré a la fuente del calor como la «caldera», y al lugar más frío donde va a parar el calor como el «disipador».)
Entonces, Carnot propone una máquina hipotética que lleve a cabo el mismo proceso pero a la inversa, es decir, que se alimente de potencia motriz para desplazar el calor de un punto frío a otro más cálido. En el mundo moderno, a este tipo de dispositivos los llamamos bombas de calor o refrigeradores. De nuevo, Carnot no muestra interés por los detalles técnicos. Se basa en el argumento de que si el flujo de calor que va desde un punto cálido hasta otro más frío es capaz de generar potencia motriz y elevar un peso, entonces puede existir una máquina que haga lo contrario. En esta máquina, la potencia motriz obtenida de un peso que cae obligará al calor a fluir «hacia arriba», desde el disipador frío hasta la caldera caliente. He aquí una analogía directa con los molinos de agua y las bombas de agua: los primeros utilizan el flujo de agua hacia abajo para generar potencia motriz, mientras que las segundas utilizan la potencia para empujar el agua hacia arriba.
Sigamos la lógica de Carnot e imaginemos un motor ideal que, al recibir 100 calorías de calor desde la caldera, eleve 10 m un peso de 50 kg y luego libere el calor a un disipador.
Imaginemos ahora el motor «inverso» ideal, en el cual, mientras un peso de 50 kg cae 10 m, se extraen 100 calorías de calor del disipador y se llevan a la caldera.
Una vez definidas estas dos máquinas hipotéticas, ahora cabe preguntarse: ¿qué pasa si las unimos? Ahora, la potencia motriz que genera la máquina ideal que va «hacia delante» es la que impulsa el motor ideal «inverso».
El flujo de calor que va desde la caldera y hasta el disipador a través del motor ideal eleva un peso.
El peso entonces se conecta con el motor ideal inverso y lo deja caer, lo que «eleva» el calor desde el disipador hasta la caldera.
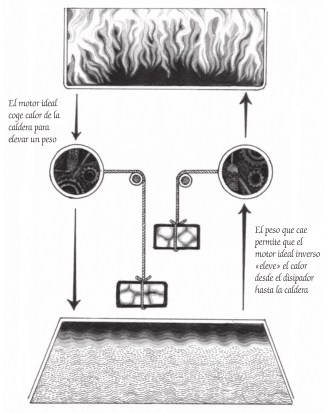
Un motor ideal impulsa un motor ideal inverso
Este sistema funcionará eternamente.12 De manera que 100 calorías de flujo de calor se desplazan desde la caldera hasta el motor que va hacia delante y terminan en el disipador, elevando el peso de 50 kg por el camino. El peso está conectado al motor inverso y lo deja caer, lo cual eleva 100 calorías de calor de nuevo desde el disipador y reabastece la caldera. Esto alimenta el motor que funciona hacia delante, lo que vuelve a elevar el peso y el bucle se reinicia y se repite.
El quid de la cuestión es que esta caldera jamás perderá calor13 y el peso subirá y bajará a perpetuidad. Pero —y aquí viene un pero de los grandes— este sistema no proporcionará ni un ápice de potencia motriz útil. El motor inverso consume íntegramente la potencia motriz que genera el motor que va hacia delante. No queda ningún remanente con el que hacer algo de utilidad, como bombear agua.
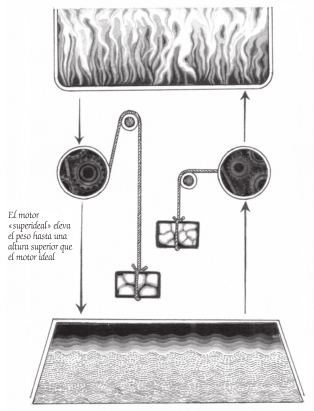
Un motor «superideal» impulsa un motor inverso ideal
El siguiente paso de Carnot tiene un punto de genialidad. Se inventa otro motor hipotético que utilice un gas alternativo que no sea vapor, como aire o vapor de alcohol, solo que el gas imaginario que propone es mejor que el vapor, lo que significa que el motor que lo emplea también es mejor que una máquina de vapor. Pero ¿hasta qué punto es mejor?14 Supongamos que eleva un peso de 50 kg a una altura de 12 m en lugar de 10 m a cambio del mismo flujo de 100 calorías de calor entre la misma caldera y el mismo disipador.
Como ya ha hecho antes, Carnot analiza el sistema en el que este motor «superideal» (que no es de vapor) impulsa el motor ideal inverso: 100 calorías fluyen hacia el motor superideal, pero dado que eleva el peso en 12 m, puede impulsar el motor «inverso» y también, por ejemplo, una bomba de agua. Al motor inverso le basta con que el peso caiga 10 m para mandar las 100 calorías de vuelta a la caldera y reabastecerla. Pero en el motor superideal, el peso todavía puede caer otros 2 m al final de cada ciclo; es decir, cae 12 m en lugar de 10 m.
Esta «distancia de caída sobrante», por llamarla de alguna manera, también podría utilizarse para bombear agua. De hecho, cada ciclo generará un excedente de «agua caída». Este tipo de máquina sería capaz de generar energía útil sin consumir ningún tipo de combustible.
Sin embargo, declara Carnot, esta máquina no puede existir. Se trata de una máquina de movimiento perpetuo, cuya existencia los científicos habían dado por imposible hacía mucho. Durante siglos, hubo quienes soñaron con construir máquinas que hicieran algo útil sin exigir estímulos o impulsos generados por animales, agua en curso o viento. Ninguna funcionó jamás, y en 1775, la Real Academia de Ciencias de París anunció que dejaba de aceptar propuestas acerca del movimiento perpetuo. En el texto en el que analizaba los molinos de agua, el propio padre de Sadi utilizó la misma presuposición de la imposibilidad del movimiento perpetuo para establecer un límite superior sobre la cantidad de trabajo útil que podía extraerse de dichos artilugios. La genialidad de Sadi Carnot residía en que se dio cuenta de que la misma lógica funcionaría, con grandes resultados, en las máquinas de vapor. Tal como escribió:
«¿No sabemos, además, a posteriori, que todos los intentos de generar movimiento perpetuo por cualquier medio han sido infructuosos? ¿Que nunca hemos logrado generar un movimiento verdaderamente perpetuo, es decir, un movimiento que siga por siempre sin alteración alguna en los cuerpos que se han puesto a trabajar para tal fin?»
Para Carnot, la inviabilidad del movimiento perpetuo significa que no es posible construir un motor que produzca más potencia motriz que una máquina de vapor ideal. O, según sus palabras:
«Esta creación va frontalmente en contra de las ideas hoy aceptadas, de las leyes de la mecánica y de la física del sonido. Es inadmisible. Por lo tanto, debemos concluir que la máxima potencia resultante del empleo del vapor es también la máxima potencia motriz alcanzable por cualquier medio.»
El propio Carnot destacó su conclusión en cursiva. Lejos de decir que el vapor es el mejor material que pueda usarse, lo que plantea es que todos los motores ideales funcionan igual de bien, independientemente del gas o de cualquier material a partir del cual funcionen y de cómo se construyan. La máquina de vapor ideal podía tener un aspecto muy distinto de un motor de aire ideal, pero cuando ponen en marcha la misma combinación de caldera y disipador, todos elevarán un peso hasta el mismo punto. Y ello significa que los materiales que hacen funcionar el motor, como el vapor o el aire, no proporcionan potencia motriz alguna por sí solos: todo procede del flujo del calor.15
Carnot había tenido en cuenta las máquinas de vapor en su forma idealizada y había sacado a relucir una certeza sobre su equivalente en el mundo real que ningún otro ingeniero había señalado. La mayoría seguían creyendo que el material que se utilizaba para hacer funcionar el motor desempeñaba un papel u otro en la generación de potencia motriz.
Para entender el razonamiento de Carnot, fijémonos en un molino de agua. Si tenemos en cuenta un flujo de agua concreto, la potencia máxima que podrá producirse está limitada por la altura a la que caiga el agua. Ningún diseño, por ingenioso que sea, podrá lograr que se exceda dicho límite. La única forma de aumentar la potencia del molino es aumentar la altura a la que cae el agua. Del mismo modo, en el caso de cualquier motor térmico, la potencia que podrá generar a partir de un flujo de calor determinado está limitada por la diferencia de temperatura entre la caldera y el disipador. La única forma de aumentarla sería incrementar la diferencia de temperatura, mientras que reducir la diferencia de temperatura disminuirá la potencia que se genere.
Carnot también analizó cómo maximizar la potencia motriz que generaba el flujo de calor a partir de una bajada de temperatura determinada. En un motor típico, el calor provoca que un gas como el vapor se expanda y empuje un pistón; en un motor ideal, todo el calor debería contribuir a expandir el gas, en lugar de perderse a causa de fugas, por ejemplo. (Para más detalles, véase el Apéndice I.)
Este razonamiento lógico llevaba a Carnot a pensar que las máquinas de vapor reales que existían en su tiempo debían de estar derrochando una gran cantidad de energía. Carnot estimaba que la temperatura más elevada que alcanzaba el vapor al expandirse y empujar un pistón era algo superior a los 160 ºC,16 mientras que la temperatura mínima que alcanzaba al condensarse era de unos 40 ºC, lo que significaba que las máquinas de vapor extraían potencia motriz de una bajada de temperatura de unos 120 ºC. Pero la temperatura en la caldera de la máquina, donde se quemaba el carbón, superaba los 1.000 ºC, lo que suponía que se estaba desaprovechando una diferencia de temperatura mucho mayor, de 900 ºC o más.
De nuevo, el molino de agua nos ayudará a ilustrarlo. Imaginemos una cascada con una caída de 10 m. Ahora imaginemos una rueda hidráulica colocada a tan solo un metro por debajo de la parte superior, en lugar de estar situada en la parte inferior. La conclusión instintiva es que se está derrochando gran parte de la potencia del flujo del agua. Las máquinas de vapor derrochan flujo de calor de una forma parecida.
¿Cómo podía corregirse esto? Carnot plantea que una forma sería utilizar el aire atmosférico como sustancia para empujar el pistón. Dado que el aire contiene oxígeno, el combustible puede arder y generar calor dentro del cilindro en lugar de en una caldera externa, como vemos en las máquinas de vapor. «Así, podría evitarse una pérdida considerable», decía Carnot. El aire tiene otra ventaja: presenta un «calor específico» más bajo que el vapor, lo que, a grandes rasgos, significa que la misma cantidad de calor puede elevar más la temperatura de una cantidad determinada de aire que de una cantidad de vapor equivalente. Asimismo, ello implica que el mismo flujo de calor puede hacer funcionar un motor a base de aire a partir de diferencias de temperatura mayores que una máquina de vapor, alcanzando, de este modo, una eficiencia aún mayor. Carnot escribe: «El uso de aire atmosférico para desarrollar la potencia motriz del calor […] ofrecería sin duda alguna una ventaja notable respecto del vapor de agua». Esta predicción surgió a finales del siglo XIX gracias a la llegada del motor de combustión interna, un dispositivo que consume petróleo o diésel para elevar las temperaturas del aire en sus cilindros hasta bien superados los 1.000 ºC. Rudolf Diesel, que publicó sus teorías sobre cómo construir este tipo de motor en 1893, se inspiró en las ideas de Carnot.17
El tratado de Carnot es una obra científica maravillosa, el resultado de una imaginación fértil que trabajaba de la mano de una mente que razonaba meticulosamente a partir de la evidencia. Estamos rodeados de su legado. Los motores de combustión interna, los reactores, las gigantescas turbinas que generan electricidad e incluso los cohetes que llevaron al hombre a la Luna parten del descubrimiento de Carnot de que, para generar potencia motriz, es necesario disponer de un flujo de calor que oscile de caliente a frío. Otro legado de la obra de Carnot, menos obvio, pero igual de importante, es su afán por entender mejor nuestro universo.
En el verano de 1824, Carnot corrió con los gastos de la publicación de Reflexiones sobre la potencia motriz del fuego a la edad de veintiocho años. Quizá habría sido más inteligente enviar su trabajo a la revista de su alma mater, la Escuela Politécnica, que contaba con numerosos lectores; pero tal vez el estilo de sus Reflexiones, una mezcla de sociología, política y razonamiento abstracto hizo que no tuviera cabida. En cualquier caso, autopublicó su obra con un coste de 459,99 francos,18 lo que debió de poner su economía contra las cuerdas si tenemos en cuenta que vivía del medio sueldo que recibía del ejército francés. Se imprimieron seiscientos ejemplares y salió a la venta el 12 de junio de 1824 al precio de tres francos por unidad. No hay registros de cuántos se vendieron. Sin embargo, ese mismo mes, una síntesis de las ideas de su libro se leyó en la Academia de Ciencias de París, aunque no hay evidencia alguna de que los científicos más influyentes de Francia recordaran dicha presentación, y ninguna prueba de que Carnot estuviera presente para defenderla.
A partir de finales de la década de 1820, Sadi Carnot se deja entrever en el agitado escenario político de Francia. En 1828, por ejemplo, abandonó el ejército francés, y desde ese momento no se tiene constancia de que tuviera ningún tipo de empleo, a excepción de una carta en la que indica que había intentado emprender un negocio como ingeniero.
En los años que siguieron a la publicación de Reflexiones sobre la potencia motriz del fuego, hay indicios de que Carnot pudo haber perdido la fe en su trabajo. Aunque apenas se conserva documentación personal, su hermano pequeño encontró una recopilación, un fajo de veintitrés hojas sueltas, titulada Notas sobre Matemática, Física y otros temas, que revelaba que Carnot albergaba dudas sobre un supuesto clave de sus Reflexiones: que el calor era un fluido indestructible conocido como calórico. Al reflexionar sobre cuándo el calor hace algo perceptible, como puede ser empujar un pistón, escribe: «La cantidad ya no puede seguir siendo constante». Echando la vista atrás, podemos leer esta preocupación como una prueba de sus impecables instintos científicos. Pero para Carnot, habría sembrado dudas sobre su idea principal, es decir que, sin el frío, el calor es inútil. Además, si el calor no es un fluido calórico que produce potencia motriz a medida que fluye de un cuerpo caliente a otro frío, el conjunto de su hipótesis se tambalea. Tal como lo expresó en sus notas: «Sería difícil explicar por qué, en el desarrollo de la potencia motriz del calor, un cuerpo frío es necesario». Y precisamente el problema de cómo reconciliar la idea de Carnot de que el calor debe fluir de un cuerpo caliente a otro frío para generar potencia motriz con su fluido calórico imaginario es donde nuestra historia da el siguiente giro.
Sin embargo, y por desgracia, a partir de este momento Carnot deja de estar implicado. En 1832, por razones que siguen siendo desconocidas, Carnot ingresó en un hospital psiquiátrico en Ivry, a las afueras de París. Durante su estancia, una epidemia de cólera arrasó toda Francia y Carnot fue una de las víctimas de la enfermedad. La última imagen que tenemos de Sadi Carnot19 es la de un hombre asolado por una fiebre alta y gran angustia mental, que se halla a las puertas de la muerte sin ser consciente de la inmensa importancia de su trabajo. En el libro de registros del hospital psiquiátrico se puede leer: «Señor Carnot Lazare Sadi, exingeniero militar, ingresado el 3 de agosto de 1832, por manía. Curado de manía. Muerto por cólera, 21 de agosto de 1832».
Tenía treinta y seis años.