2 NUESTRO MUNDO, NUESTRA ATMÓSFERA A cuarenta mil kilómetros
LA MAYOR PARTE DE NUESTRA ATMÓSFERA
Hemos llegado aquí después de un largo viaje, pero por fin hemos llegado a la Tierra. En nuestro planeta, nunca estamos a más de veinte mil kilómetros de casa, una idea seguramente tranquilizadora. Compartimos nuestra atmósfera vivificante y de proporciones perfectas con, entre otras formas de vida, unos ocho mil millones de personas. Y todas respiramos. Inhalar, espirar. Inhalar, espirar. Y, literalmente, no nos saciamos nunca. Así pues, ¿qué tiene nuestra atmósfera que la hace tan extraordinaria?
Aunque pueda parecer extraño, el aire que respiramos aquí en la Tierra contiene unas cuatro quintas partes de nitrógeno, un gas con muy poco encanto. Lo inspiramos y enseguida lo espiramos. El nitrógeno es una parte importante de nuestra vida en muchos sentidos —por ejemplo, contribuye al crecimiento de las plantas—, pero no hace gran cosa en la atmósfera. También hay una pizca de argón, más anodino aún que el nitrógeno. Como veremos, el argón pertenece al grupo de sustancias conocidas como «gases inertes», nombre que te dice todo lo que necesitas saber sobre lo que ocurre con el argón cuando respiras. Nada. Lo inhalas y lo exhalas.
Con tan poca cosa, a los científicos les costó bastante tiempo descifrar lo que hay en la atmósfera; en realidad, comprender que al aire es algo más que nada, y también que sea invisible. A decir verdad, la propia química no empezó a liberarse de los grilletes de la alquimia, su pariente indiscutible e incómodo, hasta el siglo XVII. Sin embargo, en 1774, solo unos cien años después de que se dieran los primeros pasos tambaleantes en esta nueva forma científica de analizar el mundo que nos rodea, los filósofos naturales habían identificado el 99 % de la atmósfera: tanto el nitrógeno como el oxígeno. Supuso un gran avance, sobre todo si tenemos en cuenta que el concepto moderno de gas ni siquiera existió como idea hasta la publicación en 1648 de Ortus medicinae, de Jan Baptiste van Helmont. La concreción de estos conceptos básicos resultó importante para nuestra incipiente comprensión de la atmósfera, porque todo ocurre en la quinta parte de atmósfera que no es argón ni nitrógeno. Hoy sabemos que esta parte está compuesta casi por completo de oxígeno. Casi. De hecho, gran parte de este libro gira en torno a esta dichosa palabra: «casi». Lo que me interesa es la pequeñísima parte de nuestra atmósfera que no es nitrógeno, ni argón ni oxígeno. Sin embargo, antes de abordar el tema, fijémonos un momento en el oxígeno, que hace algo más que intentar asfixiarnos.
El oxígeno estuvo a punto de recibir nombres como «aire de fuego», «aire vital» o uno de una oscuridad insuperable: «aire deflogisticado». Finalmente, lo llamaron oxígeno, cuyo significado es «formador de ácido» (algo bastante desafortunado). Preferiría que se llamara «aire vital», pero al menos nos libramos de tener que hablar de «aire deflogisticado». En el capítulo 9 hablaremos más detenidamente del flogisto y descubriremos por qué el oxígeno casi acaba por llevar este extrañísimo nombre. «Aire vital» (o tal vez «vitalio») hubiera dado en el clavo, porque el oxígeno es lo que nos da la vida. Y no ocurre solo que el oxígeno nos da vida, sino que la vida nos da oxígeno. Cuando se formó la Tierra, hace unos cuatro mil quinientos millones de años, en la atmósfera no había oxígeno. Y no sabemos aún de ningún otro planeta que contenga oxígeno en su atmósfera. No fue hasta que organismos unicelulares empezaron a producir oxígeno, al cabo de unos quinientos mil millones de años, cuando se abrió cierta probabilidad de que hubiera oxígeno en la atmósfera. Pero la realidad es que esta siguió sin oxígeno durante otros mil millones de años, porque el hidrógeno engullía todo el que producían las primeras formas de vida vegetal, o bien se consumía en la reacción con el hierro y otros materiales geológicos.1 Así siguieron las cosas durante unos mil millones de años antes de que empezara a intervenir la fotosíntesis, cuyo resultado fue una producción de oxígeno suficiente para que comenzara a acumularse en la atmósfera, al mismo tiempo que disminuía la producción de hidrógeno de los volcanes.
A partir de hace unos dos mil trescientos millones de años, los niveles de oxígeno en la atmósfera empezaron a subir por encima del 3 %, un nivel en el que siguió durante mucho tiempo. En realidad, mucho muchísimo tiempo: hasta hace unos setecientos millones de años. Más tarde, los niveles de oxígeno empezaron a volverse un poco locos. En un abrir y cerrar de ojos (en solo unos cincuenta millones de años), se produjo un aumento constante, hasta el 13 %. Lo siguió otro incremento repentino, hasta alcanzar el nivel más alto jamás alcanzado2 en el periodo Carbonífero, hace unos trescientos millones de años. Por entonces, el nivel de oxígeno en la atmósfera era un 50 % superior al actual. Como consecuencia, se desarrollaron algunas formas de vida excepcionales: libélulas del tamaño de una gaviota, arañas con patas de casi medio metro de largo y ciempiés que medían un metro de un extremo al otro.3 Unos bichos realmente terroríficos cuya viabilidad respondía al alto nivel de respiración que les permitía una atmósfera que contenía más de un 30 % de oxígeno.
Al parecer, hace unos trecientos millones de años, la causa de la subida de los niveles de oxígeno fue el rapidísimo enterramiento de los bosques, que contenían inmensas cantidades de carbono. La desaparición del carbono supuso que el oxígeno producido por la fotosíntesis no tuviera otro lugar al que ir que a la atmósfera, en cuya composición pudo alcanzar, en su punto más alto, hasta el 35 %. Sin embargo, llegaron los viejos humanos de siempre: nunca satisfechos con estar razonablemente bien, en los últimos dos mil años hemos hecho lo peor que hemos sabido para corregir ese equilibrio, desenterrando esos viejos bosques, convirtiéndolos en carbón y petróleo en nuestro propio beneficio, y quemándolos para producir calor y electricidad.
Por lo que sabemos, la Tierra es el único planeta que produce oxígeno. Así pues, aunque por ahí fuera pueda haber planetas que estén en condiciones para que en ellos evolucione la vida, no hemos encontrado ninguna prueba de la existencia de vida basada en el oxígeno. Si en algún momento hallamos otra atmósfera rica en oxígeno, podría ser, efectivamente, un sólido indicio de que la vida ha evolucionado en ese planeta, y que este trabaja en la fotosíntesis de forma denodada.
De vuelta a la Tierra, si las plantas hacen cuanto pueden para llevar oxígeno a la atmósfera, los animales ponemos todo nuestro empeño en engullírselo de nuevo. Cuando respiramos, parte del oxígeno del aire pasa a la corriente sanguínea a través de la extensísima superficie de nuestros pulmones. La superficie total de los pulmones de una persona adulta es de entre cincuenta y setenta metros cuadrados (más o menos la mitad de una pista de tenis, pero, por favor, no intentes comprobarlo en tu club de tenis). Esta gran superficie permite que el cuerpo extraiga en torno a una cuarta parte del oxígeno presente en cada inhalación. Así pues, cuando espiramos, el aire contiene alrededor de un 15 % de oxígeno. Inhalamos, 21 %; exhalamos, 15 %. Algo parecido ocurre al quemar combustibles. Como en la respiración, el proceso de quema de un combustible consiste básicamente en la reacción del carbono y el hidrógeno del combustible con el oxígeno para obtener dióxido de carbono y agua. El principio es el mismo en el motor de combustión interna de un coche o un camión, el quemador de leña del salón, la más moderna central eléctrica alimentada por gas, o tus pulmones y tu corriente sanguínea. Y las consecuencias de todo esto son muchas e importantes. De hecho, con tanta respiración y tanta quema de combustibles fósiles, extraemos oxígeno de la atmósfera a un ritmo un tanto superior a la capacidad de reponerlo de las plantas. Esto significa que actualmente los niveles de oxígeno en la atmósfera disminuyen en torno a un 0,0019 % al año.4 A este ritmo, dentro de unos quinientos años, los niveles de oxígeno en la atmósfera habrán bajado del 21 % al 20 %. Nada por lo que haya que preocuparse aún, pero tal vez convenga tenerlo en cuenta.
SIN ALIENTO
Si te interesa experimentar cómo es la vida en un medio donde escasee el oxígeno sin tener que esperar un par de milenios, una posibilidad es subir a las montañas. Mientras escribía este libro, viajé a Nepal y tuve el privilegio de cruzar el paso de Larke hacia el norte del monte Manaslu, en el Himalaya. El paso de Larke está situado a unos 5.100 metros sobre el nivel del mar, una altitud más que suficiente para sentir los cambios en los niveles de oxígeno.
A esta altura, la presión del aire es más o menos la mitad de la del nivel del suelo. Así pues, lógicamente, notaba que respiraba con dificultad al realizar actividades tan extenuantes como la de atarme los cordones de los zapatos o permanecer de pie. Tenía ciertas dificultades, pero no por ello deja de sorprender que alguien como yo, que se ha pasado los últimos cincuenta años a un par de cientos de metros sobre el nivel del mar, pudiera adaptarse a esta altitud lo suficiente para cruzar a pie el paso, incluso sonreír a la cámara, en vez de concentrarse exclusivamente en reunir un poco de oxígeno. Sí, estoy sonriendo. Aquella experiencia me hizo comprender la increíble capacidad de adaptación de nuestro cuerpo, así como lo frágil y pequeña que es la atmósfera. En dos semanas, tuve oportunidad de pasar del confort familiar de una presión de una atmósfera a la incomodidad, en algunos momentos dura, de media atmósfera, para después, al cabo de un par de días, volver a las condiciones más o menos normales. Normales para mí, quiero decir. Los componentes de nuestro equipo nepalí subían como si tal cosa hasta los 5.100 metros del paso, cargando unos veinticinco kilos en la espalda. Y aún tenían fuerzas para correr a traernos termos de té a nosotros, pobres occidentales sin un gramo de fuerzas. Es cuestión de lo que a uno está acostumbrado. Y nos podemos acostumbrar incluso a la mitad del oxígeno que obtenemos a nivel del mar.

El autor, a 5.106 metros de altitud sobre el nivel del mar, en el paso de Larke, Nepal5
Durante la caminata por el monte Manaslu, encontramos banderas de plegaria en puntos especialmente significativos, como las que se ven en la fotografía. Las banderas son de color azul, blanco, rojo, verde y amarillo, siempre en este orden. Son unos colores que representan el cielo (y el espacio), el viento, el fuego, el agua y la tierra. En esta parte de Nepal, la cultura budista tradicionalmente distingue entre el cielo y el viento. Nunca antes había pensado en tal distinción, pero me parece más que razonable, pues el cielo es claramente azul e inaprensible; en cambio, el viento es invisible, pero, al mismo tiempo, suele ser tangible. Puedo asegurar que, a medio camino de la cumbre de la octava montaña más alta del mundo, el viento es realmente tangible. Sin embargo, tanto el cielo azul como el viento invisible están compuestos de lo mismo. ¿Por qué, entonces, el cielo nos parece azul mientras que la atmósfera es transparente? La respuesta es que el color azul del cielo se debe a la dispersión de la luz solar. Siempre que no miremos directamente al sol —algo que estoy seguro de que no haremos por razones de seguridad—, la percepción que tengamos del color del cielo se deberá a que la luz del sol se dispersa al atravesar la atmósfera. El grado de difusión de la luz es inversamente proporcional a la cuarta potencia de la longitud de onda de la luz. La luz azul cuenta con una longitud de onda más corta que la verde, la amarilla, la naranja o la roja, por lo que se dispersa más: hasta diez veces más que la luz roja. Esta es la razón por la que la luz que vemos cuando miramos al cielo claro es azul: por la alta intensidad de los colores de longitud de onda más corta, los azules y los violetas. El resultado es que percibimos el cielo como de color azul. A una altitud de 5.100 metros, tenía sobre la cabeza la mitad de la atmósfera que a nivel del mar; por tal motivo, la intensidad de la luz difusa de todas las longitudes de onda era más baja que la de aquella a la que estoy acostumbrado a nivel del mar. Tal cosa provocaba que el cielo pareciera más oscuro de lo habitual en un día radiante de primavera, y de un azul todavía más profundo y que rozaba el azul oscuro o el morado fuerte cuanto más apartaba la vista del Sol.
LAS CAPAS DE LA ATMÓSFERA
El peso estimado de la atmósfera es de 5.500 billones de toneladas (una millonésima parte de la masa de la Tierra).6 Tenía a mis pies casi la mitad de todo lo que hay en la atmósfera cuando ascendí a cinco mil metros sobre el nivel del mar. La atmósfera es increíblemente pequeña, y se extiende como una capa de barniz sobre la superficie de la Tierra. No solo es pequeña y frágil, sino que, aún más importante, necesitamos que la atmósfera de nuestro planeta se quede ahí, así que tenemos que cuidarla con todo el esmero del mundo.
Pese a la altitud del paso de Larke, me encontraba solo a medio camino de superar la capa inferior de la atmósfera. Solemos dividir la atmósfera en cuatro capas, que son, de abajo arriba, la troposfera (donde se da el estado del tiempo, vivimos las personas, las aves vuelan y los hombres como yo sucumben a la crisis de la edad mediana haciendo senderismo por el Himalaya), la estratosfera (que incluye la capa de ozono y los vuelos de larga distancia), la mesosfera (por donde pasan zumbando las estrellas fugaces) y la ionosfera (con las auroras boreales y australes). Los límites de estas capas no son simples divisiones arbitrarias, sino que tienen una base física real en los súbitos cambios del perfil térmico de la atmósfera.
Partiendo de abajo, la troposfera contiene tres cuartas partes de la atmósfera. Es donde se produce casi todo lo relacionado con las condiciones atmosféricas —un poco más arriba, la situación es un poco más tranquila—. La troposfera alcanza la mayor altitud en el ecuador —unos dieciséis kilómetros por encima del suelo— y la menor hacia los polos, donde solo llega a unos ocho kilómetros sobre el nivel del suelo. A medida que se sube del nivel del suelo, la temperatura desciende unos 6,5º por kilómetro, debido a la expansión de los gases al ascender por la troposfera.
En la parte superior de la troposfera se produce un cambio abrupto de este perfil. De repente, el enfriamiento de la atmósfera se ralentiza para después cambiar de sentido. Y la temperatura empieza a subir con la altura. Esa parte superior de la troposfera (conocida como la tropopausa) se suele definir como el punto en que el ritmo del cambio de temperatura con la altura es de menos de dos grados por kilómetro, con una temperatura habitual de -60º. Este cambio del perfil térmico coloca una tapa sobre la troposfera. Donde los gases más fríos se sitúan por encima de los más calientes se pueden mezclar, porque el aire más frío baja, y el más caliente, sube (para ser más exactos, la mezcla se puede producir cuando los gases de temperatura más alta de la que resultaría la del movimiento vertical que siguiera la tasa de cambio adiabático están situados por encima de los gases más fríos, las nubes, la lluvia, los vientos). Debido en parte a su perfil térmico, la troposfera es un lugar de una dinámica fantástica, con la mezcla y el movimiento de las masas de aire, las puestas de sol y todo lo demás que la familiaridad nos ha llevado a imaginar como simples condiciones meteorológicas. Unas condiciones que, sin duda, siguen siendo muy importantes para nosotros: no contento con tener su propio programa en la televisión varias veces al día, el tiempo sigue siendo tema de conversación habitual para la mayoría de los británicos. ¿Y por qué no lo iba a ser? Ya sé que en nuestra isla ligeramente húmeda el tiempo no tiene características extremas, pero hace poco, en Edimburgo, en un mismo día hubo un sol cálido, fuertes vientos, movimientos rápidos de las nubes, lluvia torrencial, arcoíris dobles y, para concluir, una puesta de sol gloriosa. Seguramente recordarás algo parecido. Es el encanto de la troposfera. En cambio, donde los gases más calientes están por encima de los más fríos, como ocurre en la estratosfera, no se produce ninguna mezcla por inducción térmica. Las partes más ligeras y calientes de la atmósfera, y las más densas y frías, permanecen donde están. Por extraño que parezca, la previsión del tiempo en la estratosfera es aún más monótona que la de Midlands Today de la BBC.
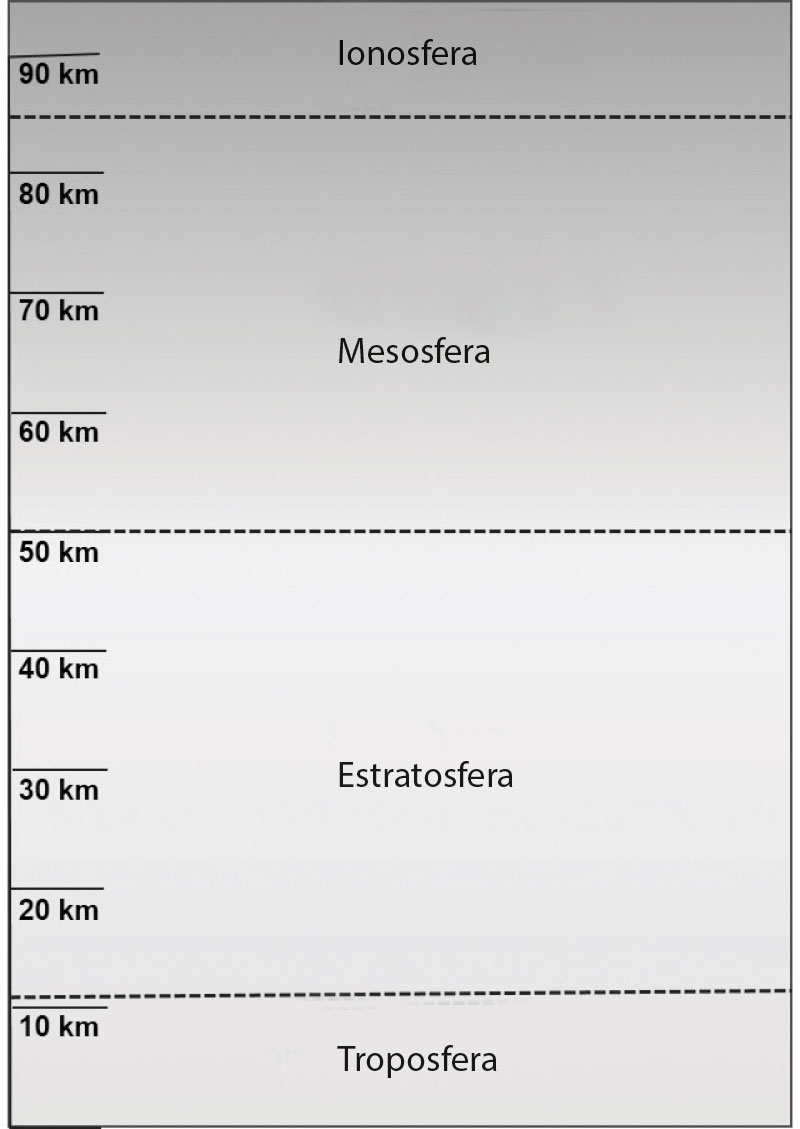
Las cuatro capas de la atmósfera de la Tierra
¿Cuál es la causa de este cambio abrupto del gradiente de temperatura de la troposfera? Una pequeña sustancia química llamada ozono, que resulta ser importante para que comprendamos cómo funciona la atmósfera y, sin duda, para nuestra propia supervivencia. Hablaremos de todo ello. Sin embargo, de momento, lo que importa es que el ozono es un buen absorbente de la luz del sol. Al absorberla, el ozono emite una radiación infrarroja de longitud de onda más larga, también conocida como «calor». De modo que donde tiene lugar este proceso hay una absorción constante de la luz del sol y una liberación de calor. El ozono se forma en la parte superior de la troposfera por la acción de la luz ultravioleta sobre el oxígeno. En ese punto, el ozono absorbe algo más de luz solar y emite un poco de calor en un proceso cíclico, antes de quedar eliminado definitivamente por los procesos químicos. La consecuencia es una zona de habitabilidad para el ozono (preferiría que la hubiésemos llamado «zona del ozono» y no «capa de ozono»), donde el equilibrio entre estos procesos es exactamente el necesario para que haya una cantidad razonable de ozono. El proceso cíclico por el que el ozono absorbe la luz ultravioleta del sol y emite calor es la causa de que la temperatura deje de bajar en lo más alto de la troposfera y al entrar en la estratosfera. Debido a este aumento repentino de la temperatura, el paso de la troposfera a la siguiente capa superior, la estratosfera, es relativamente corto. Esta tapa colocada sobre la troposfera no es del todo hermética, por lo que entre la troposfera y la estratosfera existen fugas (de no ser así, no habría razón para preocuparnos por los agujeros de la capa de ozono estratosférica, con esos molestos clorofluorocarbonos), pero es un proceso muy limitado.
Así pues, al cruzar la tropopausa llegamos a la estratosfera. La estratosfera contiene el 90 % del ozono de la atmósfera; hablaremos del ozono con más detenimiento en el capítulo 4. Muchos vuelos comerciales pasan por la estratosfera, con pocas turbulencias y prácticamente sin nubes, lo cual se traduce en un vuelo tranquilo y una buena visibilidad de lo que debajo puedan hacer las nubes de la troposfera. La próxima vez que realices un vuelo internacional, puedes entretener a tu afortunado vecino señalando por la ventanilla y decir: «¿Ve eso? Pues es la tropopausa». Nunca falla.
A medida que vamos ascendiendo por la atmósfera, la temperatura se mantiene más o menos constante, pero después empieza a aumentar con la altura. Cuando llegamos a lo más alto de la estratosfera, a unos cincuenta kilómetros del suelo, la temperatura vuelve a los húmedos -15º. Pero la sensación en ese punto no sería muy agradable, porque la presión del aire en lo más alto de la estratosfera es de solo una milésima de atmósfera. En esta zona, el ozono y su efecto calentador desaparecen. Y la temperatura de la atmósfera vuelve a bajar a medida que subimos a la mesosfera.
La mesosfera nos protege de meteoros y meteoritos, que al entrar en esta parte de la atmósfera de la Tierra arden. Las presiones extremadamente bajas del aire en la mesosfera son suficientes para calentar y, en general, destruir los objetos que se precipitan hacia la superficie de la Tierra. A estos objetos ardientes de la mesosfera los llamamos a veces «estrellas fugaces», pero, como bien sabemos, no son realmente estrellas, sino simples meteoros que se vaporizan. La mesosfera se extiende hasta unos ochenta o noventa kilómetros sobre la superficie de la Tierra. En mi trabajo sobre la calidad del aire en las partes más bajas de la atmósfera, no me suelo encontrar con la mesosfera, por lo que pensé que tal vez debiera averiguar un poco más sobre ella. Resulta que la mesosfera es una parte muy misteriosa de la atmósfera; está demasiado alta para que la alcancen los aviones o los globos, y demasiado baja para poder investigarla con los satélites. La consecuencia es que sabemos menos de la mesosfera que de cualquier otra parte de la atmósfera. Los meteoros que arden en ella provocan en esa zona unos altos niveles de átomos de hierro. En las condiciones de mucho frío de los polos norte y sur, se forman cristales de hielo alrededor del polvo producido por los meteoros quemados. El resultado son unas nubes fantasmagóricas de color azul plateado en la mesosfera. Y parece que los científicos que se dedican a la geofísica mesosférica tienen una idea extravagante de su esotérico tema de estudio, y hablan sin recato de duendecillos y elfos sin atisbo de ironía alguna (valga, como ejemplo, el artículo de 2003 de la Universidad de Alaska: «Iniciación a la imaginería de elfos, halos y duendecillos con un tiempo de resolución de 1 ms»).7 Los duendecillos, elfos y otras manifestaciones son sucesos luminosos pasajeros relacionados con las tormentas de relámpagos que se producen en las partes inferiores de la atmósfera. Los duendecillos suben y bajan (una de sus variedades se llama «duendecillo zanahoria»), mientras que los elfos irradian hacia fuera en la mesosfera. Elfos (elves) no es un acrónimo muy preciso para «Emission of Light and Very Low Frequency Perturbations Due to Electromagnetic Pulse Source» («Emisión de Luz y Perturbaciones de Muy Baja Frecuencia Debidas a Fuentes de Pulso Electromagnético»). Me pregunto si los físicos que estudian la atmósfera no son más caprichosos a la hora de poner nombres de lo que cabría esperar.
Por encima de la mesosfera, la situación es muy extraña. Entramos ahora en la ionosfera, un espacio en que no hay gran cosa. Las temperaturas suben de nuevo por la absorción de la radiación ultravioleta del Sol, cargada de tanta energía que puede separar un electrón de una molécula de otro modo estable, formando un ion cargado eléctricamente. La energía liberada en forma de calor durante estos procesos evita enfriarse gracias a la disminución de la presión. En función de la actividad del Sol, la temperatura de la mesosfera puede alcanzar los 2.000º. Entre 90 y 130 kilómetros sobre el nivel del suelo, hay una capa de átomos de sodio, formada por la acción del calor atmosférico y friccional sobre los meteoros y el polvo entrantes (cada día entran en la atmósfera de la Tierra unas treinta toneladas de polvo). En la parte más alta de la ionosfera es donde se forman las auroras boreales y australes, debido a las interacciones entre las partículas cargadas que se liberan periódicamente del Sol (el llamado «viento solar») y los átomos de la atmósfera. Es un fenómeno extraño, y más aún lo es pensar que todos estos extraños fenómenos tienen lugar muy cerca de donde vivimos. Si alguien fuera capaz de construir una carretera vertical, podrías ir en coche de tu casa al extremo superior de la mesosfera en una hora. Para entonces, tendrías a tus pies el 99,998 % de toda la atmósfera. Y si fueras ascendiendo otras dos o tres horas hasta la ionosfera, a unos cuatrocientos kilómetros de la superficie de la Tierra, deberías tener cuidado de no darte con la cabeza en la Estación Espacial Internacional.
EL RESTO DE NUESTRA ATMÓSFERA
Volvamos al nivel del suelo, donde la atmósfera está compuesta de nitrógeno más o menos inerte y, en torno a una quinta parte, de oxígeno, más activo, útil y fértil. Pero, en mi opinión, lo más fascinante de la atmósfera (mucho más) es que esa interesante quinta parte no contiene solo oxígeno. Está compuesta de cantidades mucho más pequeñas de todo tipo de sustancias químicas: las que huelen, las que pueden hacerte sentir más que agotado, las que pueden emborronarte la visión, las que reaccionan entre sí… y las sustancias que hacen que la contaminación del aire sea responsable de los siete millones de muertes prematuras al año.8 Sí, siete millones. La Organización Mundial de la Salud analizó el efecto de los factores medioambientales en la salud de todo el planeta,9 y la conclusión fue que casi una de cada cuatro muertes se debe a que las personas viven o trabajan en entornos insalubres. Algunos de los peligros medioambientales son la contaminación del aire, el suelo y el agua, el cambio climático y la exposición a sustancias químicas y a la luz del sol. Por su parte, la polución del aire es la causa de más de la mitad de las muertes debidas a factores medioambientales. De modo que la contaminación es casi tan mortífera como el tabaco (responsable también de unos siete millones de muertes al año).10 Y no solo es más grave que el tabaquismo pasivo (con algo menos de un millón de muertes al año), la obesidad (tres millones de muertes al año),11 el agua contaminada (en torno a medio millón de muertes al año)12 o los accidentes de tráfico (1,3 millones de muertes al año),13 sino más grave que todas estas causas juntas.
Y todo por culpa de una diminuta quinta parte de la atmósfera. Algo sorprendente y sobre lo que, en mi opinión, merece la pena saber un poco más. Pero ¿cuáles son estas sustancias que producen efectos tan exagerados? Pues, bueno, antes de hablar de las activas, conviene señalar unas pocas sustancias inertes más.
EL PEREZOSO ARGÓN
Conozcamos al profesor William Ramsay de la Universidad de Edimburgo, químico físico, así como una especie de experto en descubrir elementos químicos, con un total de cuatro en su haber (no está mal para una sola persona, de un total de solo ciento dieciocho elementos). Hacia finales del siglo XIX, Ramsay dio con la pista de otro componente de la atmósfera. En colaboración con lord Rayleigh, descubrió que el nitrógeno destilado de la atmósfera era ligeramente más pesado que el obtenido de las reacciones químicas. La diferencia era solo de una media milésima, pero era lo suficiente para indicar que el nitrógeno de la atmósfera estaba mezclado con algo más. Ese algo era un gas inerte al que llamó «argón», que en griego significa «perezoso». Resultó que el indolente argón constituye casi el 1 % de la atmósfera. Ramsay y sus colegas fueron descubriendo todos los gases inertes: helio, neón, argón, criptón, xenón y radón, un hallazgo de tanta importancia que obligó a rediseñar la tabla periódica para dar cabida a estos elementos nuevos y sumamente vagos. ¿Quieres saber por qué los gases inertes son tan inertes? Porque los sistemas químicos se mueven hacia sus configuraciones de menor energía. La configuración de menor energía de los átomos individuales es aquella en la que el átomo tiene capas completas de electrones de carga negativa alrededor del núcleo de carga positiva. Los átomos pueden alcanzar este estado cortando electrones de otros átomos o donando sus electrones, cuyo resultado es una partícula de carga neta negativa o positiva, llamada «ion». O también pueden llegar a este estado compartiendo con ánimo cooperativo electrones con otros átomos, de lo que deriva un enlace químico llamado «covalente». Pues bien, con los gases inertes no ocurre nada de todo esto. Ya poseen capas completas de electrones alrededor del núcleo, de modo que no quieren ser prestatarios ni prestamistas de electrones ni, desde luego, compartirlos; no, muchas gracias. Se mantienen con actitud engreída al margen, con sus capas completas, observando cómo todos los demás elementos resuelven sus diferencias. Algo así como la Suiza de la química atmosférica.
EL ÚTIL HELIO
En la atmósfera hay otro gas inerte, en cantidades mucho más pequeñas que las del argón, pero mucho más útil: el helio. Es el segundo átomo más pequeño que existe (después del hidrógeno). A este pequeño tamaño y a su naturaleza inerte se debe que sea a la vez útil y muy raro. El helio no solo se utiliza para inflar globos en los cumpleaños y para que te chirríe la voz si lo inhalas. En realidad, es una sustancia tremendamente provechosa para dirigir imanes de gran potencia. Cualquiera a quien le hayan hecho una resonancia magnética tiene razones para estar agradecido al helio, que hace que los imanes funcionen para generar imágenes IRM surrealistamente detalladas, cosa que evita esas tediosas operaciones de abrir y suturar. El helio líquido se utiliza para enfriar las bobinas magnéticas hasta unas decenas de grados por debajo del cero absoluto. Una temperatura muy muy fría: unos -250º. A esta temperatura, el alambre se convierte en superconductor, de modo que por las bobinas pueden pasar corrientes muy altas. El resultado de estas corrientes son los fuertes campos magnéticos necesarios para obtener magníficas imágenes IRM tridimensionales, de gran utilidad médica.
Sin embargo, la cuestión es que el helio, por extraño que pueda parecer para una sustancia volátil, es un producto mineral. Se produce en el suelo a partir de la descomposición reactiva de minerales que contienen uranio y torio. El helio se filtra por el suelo y sube a la atmósfera. Pese a esta fuente razonablemente importante de helio, solo constituye unas cinco millonésimas partes de la atmósfera. Podría ser mucho más, pero el helio es tan ligero que, en cualquier momento, una pequeña cantidad de él puede escapar de la gravedad de la Tierra y desaparecer en algún punto del espacio. Es un proceso lento, pero lo suficientemente rápido para, a la larga, acabar permanentemente con el helio. Así pues, aunque el helio es el segundo de los elementos más abundantes en el universo (después del hidrógeno), apenas lo hay en la atmósfera. Afortunadamente, existen reservas de helio que se han formado a lo largo de millones de años, y han quedado atrapadas debajo de rocas impermeables —de modo parecido a como se forman las reservas de gas natural—. Esto significa que se puede obtener helio como subproducto de la producción de gas natural en zonas donde hay uranio y torio. En algunas áreas, como el sur de Estados Unidos y (últimas noticias) Tanzania, el gas natural contiene mucho helio, que se puede separar del gas por destilación. Otras muchas reservas de gas contienen un poco de helio, pero en niveles tan bajos que a la compañía de gas no le sería rentable extraerlo —por lo que, sencillamente, se libera a la atmósfera y acaba perdiéndose en el espacio—. Los nuevos hallazgos en Tanzania son una buena noticia, y parece que pueden abastecer de helio durante un par de décadas. Sin embargo, el helio es sobre todo un recurso natural no renovable, y seguramente nos conviene ser precavidos en cómo lo utilizamos.
EL AGUA
Pero dejemos ya los minerales, aunque el helio, por su condición de gas, probablemente sea el mineral que más me gusta: volvamos a la atmósfera. Te habrás dado cuenta de que a veces hay una gran cantidad de agua en la atmósfera, un agua que puede pasar a la superficie de la Tierra en un proceso que los científicos de la atmósfera conocen en ciertas ocasiones como «deposición húmeda», y la gente normal, como «lluvia». La cantidad de agua presente en la atmósfera varía enormemente en los diferentes lugares y épocas. En muchas partes del mundo, la lluvia es un bien preciado que hay que recoger, conservar, cuidar y usar. En otras, incluidas las pequeñas islas húmedas del Reino Unido donde vivo, normalmente tenemos agua más que suficiente, de modo que a veces la desperdiciamos y pensamos que la lluvia es un fastidio, en especial cuando nos impide disfrutar como es debido de las vacaciones o el críquet. Y las lluvias pueden provocar grandes catástrofes, con inundaciones y corrimientos de tierras, así como efectos colaterales como la propagación de enfermedades transmitidas por el agua y el aislamiento de comunidades a las que, en esas inundaciones, no pueden llegar los productos de primera necesidad. El agua de la atmósfera, como veremos, también desempeña su papel en algunos de los importantes procesos de contaminación atmosférica. Asimismo los procesos químicos que tienen lugar en las gotas de agua y en la superficie de las nubes también pueden ser importantes (y no en menor grado para la química del ozono de la estratosfera, un tema del que nos ocuparemos en el capítulo 4).
EL DIÓXIDO DE CARBONO
La segunda de las sustancias más prevalentes en la atmósfera es el dióxido de carbono, CO2. Jan Baptiste van Helmont, la persona que reconoció el concepto moderno de gas, fue también quien, a principios del siglo XVII, se dio cuenta de que el gas que se obtiene al quemar leña o carbón se encuentra también en los alimentos fermentados. El gas debía ir a alguna parte, así que era razonable pensar que ese gas estaba también en la atmósfera. Sin embargo, hace cuatrocientos años no se entendía muy bien qué era en realidad ese gas de tan misteriosa prevalencia. Van Helmont lo llamó «gas sylvestre» o «espíritu salvaje». Un nombre fantástico con el que, de paso, Van Helmont inventó también la palabra «gas», adaptada de la griega que significa «caos». En su famoso experimento, plantó un pequeño sauce en una maceta, analizó todo lo que entraba y salía, y demostró que el árbol había aumentado setenta y cinco kilos en cinco años. Era un tanto paradójico que Van Helmont no se percatara de que la sustancia responsable de gran parte de ese aumento de peso era el mismo gas silvestre que había estudiado con resultados tan innovadores. En el siguiente siglo, Joseph Black bautizó el dióxido de carbono con el nombre más prosaico de «aire fijo». Probablemente, por la naturaleza del dióxido de carbono, «prosaico» sea la palabra correcta: no es un gas que en la atmósfera intervenga en reacciones apasionantes, por lo que hablar de «espíritu salvaje» tal vez fuera darle demasiada importancia. Sin embargo, el dióxido de carbono ha sido el último en reír, y hoy conocemos mucho mejor el papel que desempeña en el control de la temperatura de la Tierra. Hasta la propia nomenclatura ha recorrido un círculo perfecto al pasar de hablar de «cambio climático» a hacerlo de «caos climático» (y de la palabra «caos» derivó Van Helmont el neologismo «gas» para describir el dióxido de carbono).
El dióxido de carbono es un gas de efecto invernadero, circunstancia que le ha dado un gran protagonismo en la prensa en los últimos veinte años, más que a cualquiera de los contaminantes del aire más activos y de más corta vida de los que me ocupo. Dado el papel que el dióxido de carbono representa en el cambio climático, las actuaciones destinadas a limitar su nivel en la atmósfera son un elemento fundamental de las políticas climáticas. En los tiempos anteriores a la Revolución Industrial que arrancó en los inicios del siglo XIX, la concentración de dióxido de carbono en la atmósfera era de 280 partes por millón, o un 0,028 % de la atmósfera (el nitrógeno, el oxígeno, el argón y el agua constituyen, cada uno, en torno al 1 % o más de la atmósfera —para después descender mucho hasta el dióxido de carbono, con menos de un tercio del 1 %—). Desde que adquirimos la costumbre de quemar combustibles fósiles, las concentraciones han aumentado de manera constante hasta 2016, cuando la concentración global media de dióxido de carbono alcanzó oficialmente las 400 partes por millón, es decir, el 0,040 %. Es un efecto más que considerable de la actuación de una especie en la atmósfera: sin ayuda de nadie, los seres humanos hemos sido capaces de aumentar el nivel de dióxido de carbono en la atmósfera en más del 40 % en solo un par de cientos de años. Este nivel de dióxido de carbono tiene graves consecuencias para el clima global, un tema, sin duda, de grandísima importancia y del que se ha escrito profusamente. Tan importante como el cambio climático, el tema que aquí nos ocupa es sobre todo la contaminación del aire, un aspecto muy distinto y creo que menos familiar de la atmósfera. Así pues, voy a ocuparme de la política y la ciencia del cambio sin meterme en polémicas cuestiones de termodinámica.
EL CAMBIO CLIMÁTICO
Desde el punto de vista climático, el dióxido de carbono es activo, pero es químicamente inerte. Tal condición es lo que le da su larga vida atmosférica y le permite contribuir de forma tan importante al prolongado cambio climático. Gran parte del dióxido de carbono que hoy vertemos en la atmósfera seguirá en ella dentro de cien años. Esta larga vida es una mala noticia para el tratamiento de los efectos que nuestras actuaciones tienen en el clima global. Y también significa que el dióxido de carbono es otra sustancia químicamente estable de escasa incidencia en los aspectos más dinámicos de la atmósfera.
El problema no es que se haya prestado poca atención a la ciencia de la atmósfera. Desde hace más de veinte años, el papel de la atmósfera en el cambio climático es el principal tema medioambiental. Tanto que nosotros, los humildes profesionales de la calidad del aire, hemos batallado para que se escuche nuestra voz en las grandes inversiones en la ciencia climática, el control y el desarrollo de políticas. El propósito final es comprender el papel que los gases de efecto invernadero y otros aspectos de la atmósfera desempeñan en el cambio climático global (y, evidentemente, hacer algo al respecto).
Por ejemplo, desde 1993 hasta 2013, Estados Unidos invirtió más de 165.000 millones de dólares en el cambio climático.14 Es muchísimo dinero. Resulta reconfortante pensar lo eficaz que puede ser tal inversión en la reducción del dióxido de carbono atmosférico a 350 partes por millón (ppm, equivalente a 0,035%), siguiendo el consejo del profesor James Hansen de la NASA y de la Universidad de Columbia: «Si la humanidad quiere preservar un planeta similar a aquel en que se desarrolló la civilización y al que se ha adaptado la vida de la Tierra, la prueba paleoclimática y el actual cambio climático indican que habrá que reducir [los actuales niveles] de CO2 a un máximo de 350 ppm».15 El problema, sin embargo, es que las cuantiosas y continuas inversiones en investigación y mecanismos que mitiguen el impacto no han conseguido frenar el aumento de los niveles de dióxido de carbono en la atmósfera. En 2016, el nivel global medio de dióxido de carbono superó las 400 ppm, y sigue aumentando 2 ppm cada año. Pese a las grandes inversiones en investigación y mecanismos de control llevadas a cabo durante varias décadas, el aumento de los niveles de dióxido de carbono en la atmósfera no muestra signo de que vaya a disminuir.
En algunos sentidos, es mucho más sencillo ocuparse de cómo influimos en el clima global que de los efectos de la contaminación del aire. El impacto climático está relacionado, en gran medida, con la presencia de gases de efecto invernadero en la atmósfera. El principal culpable es el dióxido de carbono, responsable de unas tres cuartas partes de las emisiones anuales de gases de efecto invernadero, con aportaciones más pequeñas pero importantes del metano (16 % de las emisiones totales), el óxido de nitrógeno (6 %) y los gases refrigerantes que contienen flúor (2 %).16 Cuanto mayor es la presencia de sustancias de este tipo en la atmósfera, más probable es que esta retenga el calor y, por ello, que suban las temperaturas y se produzcan efectos imprevisibles en el clima y las condiciones meteorológicas. Desde esta perspectiva, el objetivo de la ciencia climática y de la política de mitigación debe ser la gestión de las emisiones. Una vez que un gas de efecto invernadero ha pasado a la atmósfera, es relativamente irrelevante en qué parte de ella se encuentra. La vida atmosférica de los principales gases de efecto invernadero es suficientemente larga como para que se mezclen de forma eficaz por toda la atmósfera, cualquiera que sea el punto en que se liberaron, de modo que lo único que nos interesa es la cantidad emitida (o la tasa de emisión) y la concentración global media resultante. Así de sencillo.
En cambio, la contaminación del aire es, en muchos sentidos, más difícil de tratar conceptualmente. Como ocurre con los gases de efecto invernadero, nos interesan, evidentemente, la cantidad de emisiones y la tasa de emisión, así como las consiguientes concentraciones en la atmósfera. En algunos casos, nos basta con esta información para ocuparnos del problema. (Por ejemplo, el Convenio sobre la Contaminación Atmosférica Transfronteriza a Gran Distancia de Naciones Unidas establece los límites de emisiones de contaminantes importantes para cada país signatario. El objetivo del convenio es: «Mejorar la calidad del aire local, nacional y regionalmente».17 Y para conseguirlo se fijan los límites de las emisiones anuales en todo el país. Así de sencillo).
No obstante, para gestionar la calidad del aire en un entorno complejo, debemos observar con mayor detenimiento el patrón de las emisiones, su dispersión en la atmósfera, los procesos físicos y químicos de conversión y las consiguientes concentraciones en suspensión. Este tipo localizado de análisis proporciona la información necesaria para comprender y gestionar los efectos de la contaminación del aire. Sin este detalle espacial, no tenemos forma de saber si los límites de emisiones como los establecidos en el Convenio sobre la Contaminación Atmosférica Transfronteriza a Gran Distancia bastarán para garantizar que alcanzamos los estándares de calidad del aire, y para evitar impactos excesivos debidos a los altos niveles de polución. O, al revés, tal vez los límites sean excesivos y más de los necesarios para impedir que afecten a la calidad del aire.
Evidentemente, estoy simplificando de forma sustancial la ciencia del clima, donde hay que investigar y comprender las interacciones entre la atmósfera, los océanos, la tierra, los ecosistemas y los seres humanos. Sin embargo, la idea que quiero transmitir es que la evaluación de la calidad del aire exige considerar los detalles de las emisiones a la atmósfera —localización, temperatura, velocidad y tasa de liberación—, algo que no hace la evaluación de los efectos de los gases de efecto invernadero. Nuestro trabajo consiste en estudiar las condiciones climáticas, así como los lugares en los que es posible que la gente esté expuesta a las sustancias liberadas. Quizá debamos entender los niveles de fondo de cualquier contaminante, cuyas fuentes relevantes tal vez no incluyamos por completo en la evaluación. Estos factores no son directamente reveladores para el tratamiento de los gases de efecto invernadero. Eso no quiere decir que ocuparse de estos gases no sea ya una tarea compleja. Las complejidades de los gases de efecto invernadero se deben a la necesidad de establecer inventarios claros y precisos de las emisiones, y, quizá más importante, la imperiosa necesidad de actuar en la gestión (es decir, la reducción) de las emisiones de gases de efecto invernadero.
EL TRATAMIENTO DEL CAMBIO CLIMÁTICO Y DE LA CALIDAD DEL AIRE
Nos encontramos en este punto con una correlación entre la gestión de los gases de efecto invernadero y la de la calidad del aire. El principal sistema para reducir los efectos del clima y de la calidad del aire es no liberar tanta polución a la atmósfera. Cualquier reducción de las emisiones de esos gases se traduce en unas concentraciones de ellos un tanto inferiores a las que de otro modo se producirían y, por lo tanto, un aumento ligeramente menor de la temperatura global. Asimismo, casi cualquier reducción de las emisiones de contaminantes del aire deriva en unos niveles de contaminantes en la atmósfera menores de los que habría sin esa reducción.
Todo lo cual está muy bien si se cumple. Pero, naturalmente, la principal razón de que contaminemos la atmósfera es ofrecer productos y servicios que nos benefician y añaden valor a nuestra vida. Las centrales eléctricas generan electricidad. Los coches, autobuses, trenes y aviones nos dan movilidad. La agricultura nos proporciona alimentos. Las calderas y el fuego domésticos nos dan calor, agua caliente y nos permiten cocinar. La lista es interminable. De modo que el problema no se resuelve simplemente diciendo «contaminemos menos» si esto significa decir «produzcamos menos electricidad» o «no viajemos tanto». La mejora de la calidad del aire debe situarse entre un amplio abanico de prioridades complementarias y, en algunas casos, opuestas.
Veamos con mayor detalle cómo podemos reducir la polución que provocamos. ¿Cómo podemos emitir menos contaminantes? Se puede conseguir haciendo menos, haciendo lo mismo de modo más eficiente o con apaños técnicos. En el caso de la contaminación del aire, además, en ocaciones podemos reducir los efectos mejorando las condiciones de la emisión, es decir, liberando los contaminantes a mayor velocidad, a una temperatura superior o desde un punto más elevado. Esto podría contribuir a la reducción de las exposiciones locales a fuentes cercanas de contaminantes del aire, pero no incidiría positivamente de modo particular en los gases de efecto invernadero.
Un ejemplo de reducción de las emisiones haciendo menos es el de la industria manufacturera del Reino Unido a lo largo de las últimas décadas. Tal disminución ha implicado una importante reducción de las emisiones de sustancias químicas asociadas a la actividad industrial —en particular, dióxido de azufre, como veremos en el siguiente capítulo— y ha planteado la pregunta de si se trata de una auténtica reducción o de la externalización de la polución a otros países (de la mano de la actividad industrial). A veces, cuando la mala calidad del aire lo exige, se imponen restricciones al tráfico o a la actividad industrial/ comercial para reducir el impacto durante un tiempo. Un ejemplo más positivo sería acabar con la necesidad de realizar una determinada actividad —por ejemplo, posibilitar que la gente trabaje desde su casa y no tenga que ir al trabajo y venir de él—. Pero, en general, limitar la actividad es un medio impopular de reducir los efectos. Exigir sin más a las personas o las empresas que hagan menos impone limitaciones a las oportunidades de unas y otras de actuar como deseen. A corto plazo, las limitaciones seguramente imprevisibles a la actividad producen un efecto disruptivo desproporcionado en la vida cotidiana y la productividad. En general, una economía normal fomenta la actividad productiva dentro de los límites establecidos, por ejemplo, los legales, éticos y medioambientales. Imponer restricciones a dicha actividad, aunque se pueda justificar por razones medioambientales o de otro tipo, exige inevitablemente un aparato de regulación e imposición.
Así pues, en principio, es mucho mejor conseguir mejorar la calidad del aire sin limitar lo que hacen las personas, y posibilitando que hagan de modo más eficiente lo que deseen hacer. Y la «eficiencia» incluye muchas opciones diversas. Posibilitar que la gente se desplace con otros medios que no sean el coche privado suele ser una forma eficaz de reducir las emisiones de gases de efecto invernadero y de contaminantes del aire —más aún porque este tipo de intervención se suele aplicar a enclaves urbanos, donde los niveles de contaminación ya pueden ser altos—. Algunas de las alternativas al vehículo privado son el transporte público o la mejora de las infraestructuras para poder circular en bicicleta. También una política que fomente compartir el coche puede ser positiva para la reducción de las emisiones de contaminantes y gases de efecto invernadero. En ciudades de todo el mundo se están acotando zonas de bajas emisiones, donde se penaliza a los vehículos más contaminantes, para mejorar la calidad del aire y reducir las emisiones de gases. Y las mejoras en eficiencia de procesos como las calderas domésticas, la calefacción y el equipamiento eléctrico de los espacios comerciales, suponen menos quema de combustibles y, con ello, menores emisiones de contaminantes del aire y gases de efecto invernadero.
Todo lo cual es fantástico. Con una mejor eficiencia, o una menor actividad, la mejora de la calidad del aire y la del clima pueden ir de la mano, y así potenciar las inversiones en mejores controles. Este tipo de cambio puede reportar también otra clase de beneficios, por ejemplo, un menor uso de materias no renovables, o niveles de ruido más bajos. Todo lo que puede generar múltiples beneficios suele ser una buena base para conseguir mejorar la calidad del aire.
EL TRATAMIENTO DEL CAMBIO CLIMÁTICO SIN OCUPARSE DE LA CALIDAD DEL AIRE
Gran parte de la atención a la reducción de los gases de efecto invernadero se ha puesto en el uso de energías renovables. Algunas de estas tecnologías tienen la ventaja de que sus emisiones son nulas o muy escasas, también en lo que afecta a la contaminación del aire. Las energía eólica, solar e hidráulica son realmente de emisiones cero, y la sustitución del sistema convencional de generación de energía por estas tecnologías supondría la consiguiente reducción de las emisiones de contaminantes del aire en el punto de generación. Sin embargo, la situación se complica si consideramos las tecnologías renovables que implican quemar madera, residuos agrícolas y desechos biogénicos. Son materiales con muy escasa emisión de gases de efecto invernadero. Efectivamente, la combustión de biomasa produce emisiones de dióxido de carbono, pero el carbono procede de fuentes biológicas y no de combustibles fósiles, por lo que no se considera que el dióxido de carbono que emite la quema de materiales biológicos contribuya de forma general a las emisiones de gases de efecto invernadero. El carbono de la madera procede del dióxido de carbono de la atmósfera y, antes o después, volvería a ella de nuevo como dióxido de carbono, de modo que la quema de madera no afecta a este proceso cíclico general. Simplemente, el proceso de combustión asegura que se produzca más pronto que tarde. Esto significa que (más o menos) podemos descartar que el dióxido de carbono derivado de la combustión de materia orgánica contribuya a las emisiones de gas de efecto invernadero.
Sin embargo, estas amables fuentes de energía de biomasa no son de emisión totalmente cero desde el punto de vista de la contaminación del aire. Desde la estufa de leña que tengo en la sala de estar hasta la última ola de digestores anaerobios de las granjas y las fábricas de alimentos, la combustión de biomasa sí emite auténticos contaminantes del aire. Y en el caso de estos contaminantes no podemos hacer distinción alguna entre fuentes biológicas y fuentes fósiles: los contaminantes que emite la combustión de biomasa son lo que son. No compensan nada lo que pudiera ocurrir si no se contara con ella. En muchas partes del mundo, la combustión doméstica a pequeña escala de biomasa como la madera y el estiércol de los animales contribuye de forma importante a la exposición a la contaminación del aire, tanto en recintos cerrados como al aire libre. Como ocurre con la cocina y la calefacción, la quema de madera en fábricas de tamaño medio para generar calor, electricidad o, lo más deseable, ambas, es una práctica presente en todo el mundo. Es posible que la quema de biomasa no genere mucho carbono, pero sí mucha contaminación. Hay que manejarla con cuidado.
EL TRATAMIENTO DE LA CALIDAD DEL AIRE SIN OCUPARSE DEL CAMBIO CLIMÁTICO
Debido a los problemas que plantea reducir la actividad y mejorar la eficiencia, en los últimos veinte o treinta años gran parte de la atención al control de la polución se ha centrado en apaños técnicos. Por ejemplo, tecnologías de combustión de bajas emisiones en centrales eléctricas alimentadas con gas, diseñadas para reducir la producción de contaminantes del aire. O los convertidores catalíticos, o catalizadores, y los retenedores de partículas en el tubo de escape de los coches, que eliminan los contaminantes una vez que se han formado. Los arreglos técnicos y las mejoras suelen ser una magnífica solución, pero una energía que emite poco carbono no es necesariamente una energía de bajas emisiones, de manera que las soluciones basadas en emitir poco no son necesariamente de baja emisión de carbono.
La solución más importante de la contaminación del aire que se ha aplicado en los últimos treinta años es el uso de catalizadores de tres vías para reducir las emisiones de contaminantes del aire de los coches de gasolina. En Europa se ha conseguido con la imposición de estándares cada vez más estrictos para los coches fabricados a partir de 1993. No existe una obligación legal específica, pero no hay otra forma de atenerse a los límites de emisiones obligatorios. La figura muestra la eficacia de la tecnología catalítica y otras mejoras en la reducción de emisiones del tráfico rodado, a pesar del aumento de la cantidad de coches desde esa época. De 1970 a 1990, la cantidad de vehículos y la de contaminantes emitidos por ellos subió de forma constante. A partir de 1990, la cantidad de vehículos ha ido siempre en aumento, pero las emisiones de contaminantes del aire de ese tráfico rodado han ido en sentido completamente opuesto. Basta observar el cambio radical de tendencia en las emisiones de monóxido de carbono del tráfico rodado en 1990.
Así pues, los catalizadores han sido otra historia de éxito, con importantes y continuas reducciones de las emisiones de monóxido de carbono, óxidos de nitrógeno y compuestos orgánicos volátiles (conocidos universalmente por las siglas ingleses VOC). El número de vehículos que rodaban por las carreteras en 2014 era dos veces y media superior al de 1970, pero las emisiones contaminantes de estos vehículos de 2014 fueron menos de la mitad de las de 1970 (cuando yo tenía tres años y me fui a vivir a la ciudad, Essex, hogar del Ford Capra, dispuesto a gozar de las delicias de los más exquisitos tubos de escape de Londres). En efecto, las emisiones de hidrocarburos debidas al tráfico rodado en 2014 fueron solo el 5 % de las de 1970. Es una desvinculación de la polución del crecimiento económico de la que hay que alegrarse.
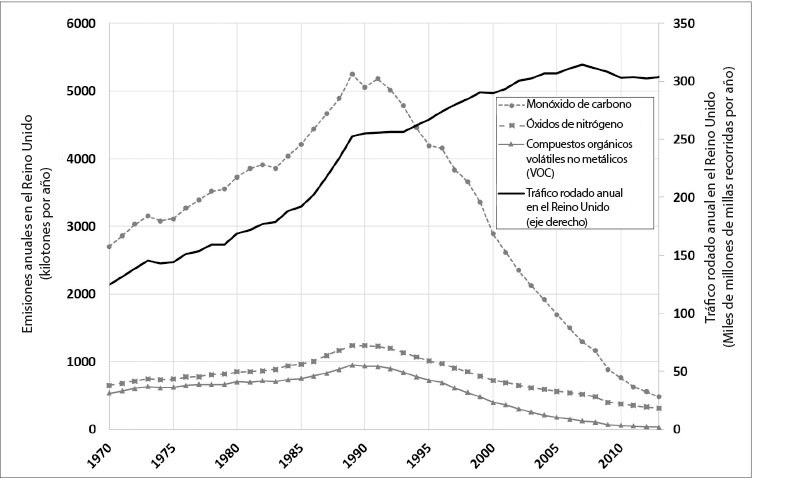
Kilometraje y emisiones del tráfico rodado en el Reino Unido, de 1970 a 201318
Las reacciones fundamentales que se producen en un convertidor catalítico son la oxidación del monóxido de carbono y los hidrocarburos para formar dióxido de carbono y agua, y la reducción del monóxido de nitrógeno y el dióxido de nitrógeno para formar nitrógeno, todas ellas sustancias inertes desde la perspectiva de la contaminación del aire.
2CO + O2 → 2CO2 + O
CxHy + (x+y/4)O2 → xCO2 + (y/2)H2O
(CxHy representa un hidrocarburo con x átomos de carbono, e y átomos de hidrógeno)
2NO → N2 + O2
2NO2 → N2 + 2O2
El catalizador es una sustancia que aumenta la velocidad de una reacción química, sin que él cambie durante la reacción. En el caso del convertidor catalítico, el catalizador es un metal perfectamente dividido con una elevada área superficial —o, de hecho, dos metales: uno para acelerar la oxidación del monóxido de carbono y los compuestos orgánicos volátiles, y el otro para acelerar la reducción del NO y el NO2—. Los gases se adhieren a la superficie del catalizador, y la presencia del metal reduce la barrera energética para que se produzca cada reacción.
Unos párrafos antes, me refería de pasada a que uno de los efectos secundarios del convertidor catalítico es convertir el monóxido de carbono y los compuestos orgánicos volátiles en dióxido de carbono, que es un gas, evidentemente, de efecto invernadero. De modo que los catalizadores han sido extraordinariamente útiles para reducir la contaminación del aire, pero también tienen sus defectos si se consideran las emisiones de gases de efecto invernadero de los coches. Y aún un tanto peor, porque la colocación de un catalizador en el extremo del tubo de escape dificulta que el motor expulse los gases de salida. El motor ha de trabajar un poco más, por lo que es menos eficiente de lo que sería de no estar ahí el convertidor catalítico. La eficiencia ligeramente menor es otro pequeño defecto en lo que se refiere a las emisiones de gases de efecto invernadero. Pero, en conjunto, no hay duda de que los convertidores catalíticos, literalmente, salvan vidas.
Junto con el uso hoy generalizado de los catalizadores, los motores de los vehículos no han dejado de perfeccionar su eficiencia y su diseño para reducir las emisiones de gases de efecto invernadero y contaminantes del aire. Y hay más (quiero decir, menos) por llegar, con el compromiso de dejar de vender coches de gasolina y gasóleo en 2040 en el Reino Unido y otros muchos países —hablaremos más de este tema en el capítulo 10—. Menor emisión no significa, por supuesto, emisión cero, o, al menos, todavía no. El tráfico rodado sigue siendo una importante fuente de gases de efecto invernadero y de polución. En todo el mundo, supone el 14 % de las emisiones anuales de gases de efecto invernadero;16 la mayor parte del resto procede de la industria, la producción de electricidad y calor, y la agricultura. En Londres, por ejemplo, en 2013, el tráfico rodado fue el responsable de más o menos la mitad de las emisiones de material particulado (partículas en suspensión) y óxidos de nitrógeno (de lo cual seguiremos hablando en el capítulo 3 y gran parte del resto del libro), y de en torno al 30 % de las emisiones de dióxido de carbono.19 Las previsiones para 2030 son que las emisiones de óxidos de nitrógeno se reduzcan aún más, en casi un 80 % —una magnífica noticia si se cumplen dichas previsiones, en particular teniendo en cuenta la reducción del 76 % ya conseguida desde el pico de 1990—. Sin embargo, el dióxido de carbono y las partículas en suspensión de los vehículos son de más difícil tratamiento, y entre 2013 y 2030 solo se prevé una ligera mejoría en las emisiones. Una de las razones es que parte de las partículas en suspensión procede de fuentes distintas de las emisiones de los tubos de escape: el desgaste de los neumáticos y los frenos, así como el polvo que los coches levantan de la superficie de la carretera. Estas fuentes requieren sistemas de control y de reducción de las emisiones completamente distintos de los utilizados en el caso de las emisiones de escape.
EL FUTURO DEL IMPACTO DEL CAMBIO CLIMÁTICO Y LA CALIDAD DEL AIRE
Algunas de las mejoras necesarias para reducir aún más las emisiones de contaminantes del aire de los coches irán de la mano de la reducción de las emisiones de gases de efecto invernadero. Los coches de mejor eficiencia energética (probablemente) emitirán menores niveles de todos estos contaminantes, tanto los del aire como los gases de efecto invernadero. Otras mejoras podrían requerir una solución intermedia entre la reducción de los gases de efecto invernadero y la de contaminantes del aire, exactamente igual que hicimos con los convertidores catalíticos hace treinta años.
El diseño de los motores de los vehículos no es lo único importante. La contaminación del aire depende de cómo, y cuánto, se conduce el vehículo. Reducir la demanda del tráfico rodado sería fantástico tanto para el clima global como para la calidad del aire local —unos beneficios medioambientales, sin embargo, que hay que considerar teniendo en cuenta la realidad en su conjunto—. Utilizar el coche particular es una decisión del consumidor. Para muchas personas, poder moverse con su automóvil es un componente esencial de su calidad de vida. El coche da acceso a la escuela, al trabajo, a los amigos, a la atención médica, a las actividades de ocio, todo lo cual cumple su función en la salud y el bienestar generales de la sociedad. A estos beneficios hay que contraponer los inconvenientes de este tipo de transporte, entre ellos, además del impacto de la contaminación del aire y los gases de efecto invernadero, el riesgo de accidentes, la ruptura de la comunidad y el impacto visual.
Una forma de reducir el uso del coche y sus efectos es aumentar el coste del transporte privado. Es algo que ya se hace con la tasa de congestión que se aplica en Londres Centro, que con sus 11,50 libras diarias ha sido completamente efectiva para disuadirme de usar el coche por el centro de Londres en horas punta para ir a la universidad a recoger a mi hijo. Un aumento más generalizado del coste del uso de las carreteras o la subida del precio de la gasolina sería, imagino, tan impopular que supondría el suicidio político de quien aplicara una política seria en ese sentido. Subir los impuestos de los carburantes nos afectaría de forma importante casi a todo el mundo, lo cual implicaría una pérdida de votos para quien implementara tal medida.
Aunque…, hablando como miembro nada representativo del electorado (y, además, sin experiencia alguna en política fiscal), subir los impuestos de los carburantes me parece, en principio, atractivo, porque sería fácil de administrar, afectaría sobre todo a los vehículos mayores y más contaminantes, dependería del uso que se haga del coche, y, si se quiere, podría vincularse a los costes más amplios de la contaminación y las emisiones de gases de efecto invernadero de los coches. Naturalmente, el sistema afectaría a todos los usuarios de vehículos, tanto a quienes deciden usar su coche como a quienes no tienen más opción que hacerlo. Es interesante que el coste de un litro de gasolina en el Reino Unido es hoy, en términos reales, muy similar al de 1983,20 y en todos esos treinta y cinco años el precio nunca ha variado más de en torno al 25 %. De modo que, pese a todas las repetidas protestas por el precio de los carburantes, en especial las de los años 2000, 2005 y 2007, subir sus impuestos es un experimento que realmente nunca hemos intentado. ¿Convendría tenerlo en cuenta?
Pensando en cómo conducimos nuestros coches, más que en cuánto los utilizamos, se han impulsado recientemente iniciativas centradas en el control del límite de velocidad. Nos hemos ido familiarizando con los controles de velocidad en las carreteras, y todo lo que contribuya a aminorar la velocidad evita la aceleración excesiva y el uso de los frenos, y disminuir la congestión será bueno también para combatir la polución.
¿Y las zonas con límite de velocidad? Por ejemplo, en la mayor parte de las calles de Edimburgo, la velocidad máxima permitida actualmente es de veinte millas por kilómetro. Veinte millas son más que suficientes, o eso dicen, lo cual es fantástico para mejorar la seguridad del tráfico, pero ¿es posible que conducir a menor velocidad implique que el motor funcione con menos eficiencia, y aumenten las emisiones de contaminantes del aire y de gases de efecto invernadero? Bien, la realidad es que las pruebas de que se dispone apuntan a que hay una enorme diferencia entre las emisiones que se producen en una zona de 20 mph y otra de 30 mph; de hecho, la de veinte millas puede generar menos emisiones de material particulado.21 Lo importante es evitar obstáculos que inciten a acelerar o frenar, algo igualmente perjudicial para la calidad del aire y la suspensión del coche.
Como ocurre con muchas medidas de gestión de la calidad del aire y del clima, estos controles de la velocidad de los vehículos no están pensados primordialmente para reducir las emisiones. Los beneficios para la atmósfera son un efecto secundario de la seguridad vial o las medidas de mejora de la velocidad. Algo que no tiene nada de malo, siempre que, con todos los demás beneficios, se entiendan y se aprovechen plenamente las oportunidades de garantizar la calidad del aire y los beneficios climáticos.
Tal vez solo acabemos por vincular el problema de la contaminación del aire y el del cambio climático cuando empecemos a quedarnos sin combustibles fósiles —o quizás un par de cientos de años después de que esto ocurra, para que el dióxido de carbono de la atmósfera tenga tiempo de disminuir nuevamente—. Tenemos reservas de combustibles fósiles para muchas décadas, así que el final de esos combustibles, con todo lo desconocido que pueda conllevar, no se va a producir en un futuro inmediato. Pero cuando se produzca, ¿qué podremos esperar?: ¿guerras energéticas?, ¿una suave transición a energías renovables?, ¿la vuelta a una sociedad de la Edad de Piedra? Aún tenemos la oportunidad de hacer factible este proceso de transición, inventando nuevas tecnologías, redescubriendo o adaptando antiguas, y quizá cambiando nuestras expectativas sobre la disponibilidad de una energía barata. Volvamos dentro de quinientos años a ver cómo nos las hemos apañado.