1
¿Cómo quieres vivir tu vida?
Hay que aprender a vivir en la inmortalidad del instante.
JOËL DE ROSNAY
Hay quien nace ya viejo, mientras que algunas personas parecen vivir una eterna juventud. ¿Cuál es su secreto? ¿Se puede llegar a centenario gozando de salud y felicidad? Estamos convencidos de ello, pero no esperes a ser viejo para reflexionar al respecto. Una vejez armoniosa es algo que requiere preparación.
¿QUÉ ES EL ENVEJECIMIENTO?
El envejecimiento es un fenómeno normal que aparece al comienzo de la edad adulta. Nos referimos al envejecimiento fisiológico del organismo, ya que el envejecimiento celular empieza poco después del nacimiento. En el organismo, el envejecimiento se manifiesta mediante una acumulación de pequeños cambios aleatorios y progresivos que afectan al conjunto de sus estructuras y funciones. Tales modificaciones, con frecuencia sutiles, se desarrollan bajo la presión de factores intrínsecos (nuestro bagaje genético) y ambientales (hábitos de vida, contaminación, estrés, etc.). El envejecimiento afecta a nuestras interacciones sociales y a la manera en que nos perciben los demás. El envejecimiento no es sinónimo de vejez, pero allana el camino a esta al incrementar nuestra vulnerabilidad a los accidentes y las enfermedades.
Ahora bien, ¿por qué envejecemos? Lo cierto es que no se sabe con certeza. No obstante, existen algunas teorías que aportan, cada cual a su manera, su pequeño fragmento de explicación.
PRINCIPALES TEORÍAS DEL ENVEJECIMIENTO
El desgaste del tiempo
Esta teoría, una de las más antiguas, contempla el envejecimiento como el resultado del desgaste por obra del tiempo y de los abusos que cometemos, un fenómeno que estaría en cierto modo preprogramado desde el nacimiento. Se trata de una visión puramente mecanicista que en realidad no tiene en cuenta el sorprendente potencial de regeneración del cuerpo humano.
Las mutaciones
Nos referimos a las modificaciones accidentales o provocadas desde el exterior, que afectan a las células no directamente ligadas a la reproducción. La idea general que subyace en esta teoría es que, dado el gran número de veces que las células de nuestro cuerpo se ven obligadas a dividirse, es normal, desde el punto de vista estadístico, que sobrevengan errores esporádicos cuando el ADN celular se copia. En general, los genes imperfectos que resultan de ello no suponen el menor problema o son reparados con rapidez por el organismo. No obstante, puede ocurrir que las mutaciones introducidas superen la capacidad reparadora de las células implicadas y tengan consecuencias importantes en el funcionamiento normal del órgano al que van ligadas. Con el tiempo, las mutaciones de ese tipo se acumularían, causando o acelerando el envejecimiento. Las intervenciones externas que favoreciesen la reparación o la protección del ADN podrían retrasar este aspecto del envejecimiento.
El envejecimiento celular
Esta teoría fue elaborada por Leonard Hayflick en los años sesenta. Dicho investigador había observado que las células de la piel que se cultivan en laboratorio solo se desdoblan un número limitado de veces, y luego suspendían el crecimiento. Es lo que se conoce como la meseta de Hayflick. Postuló que esta progresión hacia el estancamiento del crecimiento sería el comportamiento inherente a todas las células en curso de envejecimiento. Sin embargo, trabajos recientes han demostrado que es posible modular el ritmo de las divisiones celulares mediante intervenciones externas, como la nutrición.
El acortamiento de los telómeros
Se trata de una teoría reciente que viene a completar la del envejecimiento celular. Corresponde a un biólogo ruso (Aleksei Olovnikov) el mérito de haber establecido la correlación, en 1971, entre el límite de las células en cultivo observado por Hayflick y una erosión progresiva de los telómeros. Estas estructuras son fragmentos de ADN repetitivos que sirven de protección en el extremo de los cromosomas e impiden que las hebras de ADN libres se fusionen. Asimismo, evitan que la información contenida en los cromosomas se pierda durante la replicación del ADN celular. En efecto, la replicación del ADN nunca es completa en los extremos. Como el telómero recibe el impacto, el ADN codificador permanece íntegro. Ahora bien, los telómeros se degradan progresivamente con cada división celular y también se acortan por efecto de la edad, la inflamación y el estrés. Cuando ya no queda telómero, la célula deja de replicarse y entra en senescencia (sus funciones se degradan). Es lo que les ocurre, con el tiempo, a las células diferenciadas. Por el contrario, las células germinales (implicadas en la reproducción), las células madre (células de reserva, no especializadas) y las células cancerosas se benefician de la acción regeneradora de una enzima, la telomerasa. Dicha enzima, capaz de recrear los extremos que los telómeros pierden, presenta gran interés para la medicina antienvejecimiento y anticáncer.
Los ataques de los radicales libres
Los radicales libres son moléculas que han perdido un electrón. Como por lo general los electrones van en pareja, cuando uno de ellos se encuentra de pronto solo en el seno de una molécula, trata desesperadamente de volver a formar pareja. Para ello no vacilará en robar un electrón a una molécula contigua, con lo cual origina una reacción en cadena que puede resultar muy perturbadora para la célula. Por lo general se acepta que, debido al daño que pueden causar a las proteínas, los lípidos y el ADN de las células, los radicales libres contribuyen decisivamente al envejecimiento. Al retirar electrones de los componentes celulares, los radicales libres los oxidan, lo que en cierto modo provoca la «herrumbre» de los sistemas biológicos. Sin embargo, al igual que el oxígeno del que derivan, los radicales libres son necesarios para la vida. En especial, ayudan al organismo a defenderse contra las bacterias y favorecen la cicatrización. Los radicales libres solo resultan nefastos cuando su producción deja de estar compensada por los antioxidantes que el organismo produce de forma natural. Lo destructor es su exceso y su persistencia. Resulta tentador pensar que un aporte externo suplementario de antioxidantes podría contribuir a restablecer y mantener el equilibrio oxidantes/antioxidantes, pero eso está por probar.
El desajuste de la actividad mitocondrial
Las mitocondrias son estructuras especializadas que se encuentran en la mayoría de nuestras células. Se trata de verdaderas fábricas que consumen oxígeno y nutrientes para producir una molécula denominada adenosín trifosfato (ATP). El ATP es el carburante de las células; contiene la energía que necesitan para sobrevivir y funcionar de manera adecuada. Lamentablemente, al producir el ATP, las mitocondrias generan radicales libres. Y, por otra parte, las mitocondrias son especialmente vulnerables a los radicales libres. Con la acumulación de los ataques de los radicales, con el tiempo aparecen mutaciones en el ADN de las mitocondrias. De resultas de ello su actividad se ve perturbada, lo que las lleva a producir menos energía pero cada vez más radicales libres. De este modo se crea un bucle de retroacción negativa, que precipita la disfunción mitocondrial y el envejecimiento celular. Los desajustes de la actividad mitocondrial se han asociado con diversas patologías degenerativas relacionadas con la edad, como las enfermedades de Parkinson y de Alzheimer, la esclerosis lateral amiotrófica, así como algunas afecciones cardíacas. No obstante, con el descubrimiento de las células madre y de su potencial regenerador, los investigadores confían en que pronto lograrán normalizar las mitocondrias disfuncionales.
Los déficits neuroendocrinos
La producción hormonal declina con la edad. A los treinta años uno no es viejo, pero ya sintetiza menos hormona del crecimiento, lo que reduce la masa muscular y favorece la acumulación de grasa. En la menopausia y la andropausia, son las hormonas sexuales las que nos abandonan, afectando a nuestra libido y nuestro nivel de energía, al tiempo que se acelera el proceso de envejecimiento en todo el cuerpo. Otras hormonas, como la dehidroepiandrosterona, la melatonina y las hormonas tiroideas, se ven asimismo afectadas, con consecuencias similares. Los niveles de diversos mensajeros producidos por las neuronas (dopamina, ácido gamma-aminobutírico, noradrenalina, acetilcolina y serotonina) caen igualmente, perturbando el funcionamiento normal del cerebro. Por el contrario, los niveles de cortisol (la hormona del estrés) tienden a aumentar. Los niveles de cortisol crónicamente elevados desorganizan las funciones cerebrales y debilitan el sistema inmunitario. Aún está por determinar si todos esos cambios deben considerarse causas o consecuencias del envejecimiento, pero lo que sí es seguro es que las fluctuaciones neuroendocrinas contribuyen a la aparición de numerosos signos que este lleva asociados. Las terapias hormonales de sustitución pueden atenuar algunos de esos efectos.
El declive inmunológico
Es bien sabido que el sistema inmunitario funciona peor con la edad. Al envejecer, las células inmunitarias reconocen más difícilmente las sustancias extrañas (los antígenos) y los microbios. Por el contrario, las reacciones autoinmunes, dirigidas contra nuestro propio cuerpo, tienden a aumentar. El timo desempeña un importante papel en este descenso de las funciones inmunitarias. El timo es una pequeña glándula situada debajo del esternón, en cuyo interior maduran los linfocitos T. Estas células inmunitarias tienen como cometido librarnos de las bacterias y de las células cancerosas. Lamentablemente, el timo empieza a atrofiarse en una fase bastante temprana de la vida. Al llegar a los veinticinco años, dicha glándula casi ha perdido ya el 30 % de su masa, y a los sesenta ya no queda gran cosa. Esta involución del timo y la pérdida de las hormonas que sintetiza se asocian con una mayor susceptibilidad a las infecciones, al cáncer y a las enfermedades autoinmunes. En ocasiones se administra un cóctel de hormonas diversas, citoquinas y péptidos tímicos, con el fin de revitalizar el timo en las personas mayores o en aquellas cuyo sistema inmunitario se halla debilitado.
La glicación de las proteínas
La glicación de las proteínas es otro mecanismo ligado al envejecimiento. La glicación implica el añadido no enzimático de azúcares a las proteínas. En un primer momento, ciertos azúcares como la glucosa o la fructosa se fijan sobre algunos aminoácidos que encontramos en la estructura de las proteínas. Esta reacción depende de la concentración de glucosa en sangre, así como del tiempo de exposición al azúcar. En consecuencia, los diabéticos son especialmente vulnerables a la glicación. Una vez formado, el conjunto proteína-azúcar sufre diversas modificaciones químicas que dan lugar a la formación irreversible de un producto pardusco denominado AGE (advanced glycation end product, producto terminal avanzado de glicación). La reacción es bien conocida en el campo de la alimentación: las carnes a la plancha, los asados y las patatas fritas deben su oscurecimiento a ese tipo de reacción. Esto equivale a decir que, con la edad, las proteínas de nuestras células se caramelizan, lo cual no es nada bueno. Debido a la glicación, las proteínas se vuelven rígidas y se favorece la formación de aglomerados. Al verse alterada su estructura, esas proteínas ya no son capaces de asumir de manera adecuada sus funciones. Así, la glicación contribuye a la formación de cataratas en las personas mayores. Modifica asimismo la inmunogenicidad de las proteínas. Altera hasta tal punto la estructura de las proteínas que el organismo tiende a considerarlas cuerpos extraños y a atacarlas. Por fortuna, hemos llegado ya a identificar varios productos capaces de prevenir la formación de los AGE, como la aminoguanidina y la carnosina. Sin embargo, todavía no se han descubierto moléculas que puedan invertir eficazmente la glicación.
La acumulación de desechos
La actividad celular genera toda clase de desechos, incluyendo proteínas dañadas y componentes defectuosos. La célula dispone de un mecanismo para hacer la limpieza de los elementos indeseables: la autofagia. Dicho proceso moviliza una pequeña estructura esférica (llamada lisosoma) que se encuentra en la parte líquida (el citosol) de las células. A escala celular, los lisosomas son más o menos el equivalente de nuestro estómago. Tienen un pH ácido y contienen enzimas capaces de digerir prácticamente todas las moléculas biológicas. Los lisosomas reconocen las estructuras celulares y las proteínas disfuncionales, las engloban y las destruyen. Como muchos otros procesos, la autofagia pierde eficacia con la edad. Los desechos tóxicos se acumulan entonces en las células, conduciendo a su muerte prematura, por apoptosis (una especie de suicidio celular). Así, ciertas patologías neurodegenerativas ligadas a la edad y caracterizadas por la acumulación de agregados intracelulares tóxicos, como el Alzheimer, el Parkinson o la esclerosis lateral amiotrófica, se asocian a un retardo de la autofagia. En cambio, cosa que resulta interesante, es posible estimular este proceso mediante el ayuno. En efecto, ahora sabemos que los efectos beneficiosos de la restricción calórica sobre la longevidad pasan, al menos en parte, por una estimulación de la autofagia. Con la profundización de los mecanismos que controlan la autofagia, tal vez en un futuro próximo lleguemos a identificar nuevas moléculas capaces de retardar la aparición de los signos de envejecimiento. En todo caso, se trata de una vía prometedora.
¿ES POSIBLE FRENAR EL ENVEJECIMIENTO?
En los últimos años se han producido avances médicos y científicos muy alentadores en ese sentido.
La epigenética: genes bajo influencia
Desde Darwin, y hasta época muy reciente, se creía en la fatalidad de los genes. En la lotería parental, heredaríamos genes más o menos beneficiosos que determinarían nuestra susceptibilidad a las enfermedades, fijando así un límite a nuestra esperanza de vida individual. Los genes más favorables para la perpetuación de la especie, en un medio dado, se seleccionarían de forma natural mediante la supervivencia predominante de los individuos portadores y la transferencia de su material genético a las generaciones siguientes. Esta visión monolítica tuvo que ser modificada recientemente a raíz de la secuenciación del genoma humano, concluida en 2003. Para su inmensa sorpresa, los investigadores constataron entonces que solo el 2 % de nuestro ADN codifica efectivamente las proteínas que el cuerpo necesita para su supervivencia. ¿De qué sirve, pues, el 98 % restante? En 2012, los resultados del proyecto ENCODE, que implicó a más de cuatrocientos cuarenta científicos de todo el mundo durante casi cinco años, pusieron de manifiesto que la mayoría de ese ADN que no genera proteínas sirve, de hecho, para controlar la actividad de los genes que sí lo hacen. De ese modo, la actividad de los genes codificadores puede ser regulada rápidamente y con una exactitud inaudita sin implicar mutación. Dichas observaciones dieron origen a la ciencia de la epigenética, que es el estudio de la modulación de la expresión de los genes en ausencia de mutación. Los cambios epigenéticos son complejos e implican una variedad de reacciones químicas y bioquímicas capaces de activar o de reprimir la expresión de un gen.
En la actualidad está establecido que ese gigantesco cuadro de mandos, con su multitud de interruptores, responde a los cambios en nuestro estilo de vida. Lo que comemos, el ejercicio que practicamos (o no), nuestra gestión del estrés, el medio ambiente en que vivimos, la calidad de nuestro sueño, nuestra red social, nuestros pensamientos, nuestra autoestima, nuestra capacidad para experimentar placer son otros tantos elementos susceptibles de influir en el comportamiento de nuestros genes.
Nuestro código genético constituye en cierto modo un «libro cuyo protagonista somos nosotros». ¿Recuerdas aquellos libros-juego tan populares entre los jóvenes en los años ochenta y noventa? Para los que no los conozcan, se trata de libros interactivos cuyos párrafos están numerados. Al final de un párrafo, el lector puede elegir entre varias posibilidades para la siguiente acción de su protagonista. Su elección, a la que va asociado el número de un nuevo párrafo, lo lleva a otro lugar del libro donde se desarrollan las consecuencias de la opción que ha tomado. Así, con el mismo libro en mano, dos lectores dados jamás leerán la misma historia. Igual ocurre con el código genético. Dos gemelos idénticos con exactamente el mismo bagaje genético inscrito en sus cromosomas acabarán por adquirir características diferentes, porque habrán vivido experiencias distintas que han supuesto una lectura divergente de sus genes. Por ejemplo, una gemela carnívora podría desarrollar un cáncer de mama a los treinta años y la otra, vegetariana, vivir en perfecto estado de salud hasta edad avanzada, aunque ambas posean el mismo gen defectuoso asociado al desarrollo precoz de esa enfermedad. Huelga decir que se trata de un ejemplo simplificado. El cáncer es una enfermedad multifactorial, y el mero hecho de ser vegetariano no necesariamente preserva de ella. Para retomar la metáfora imaginada por Joël de Rosnay (científico y escritor de renombre), «el ADN es como una partitura musical que se transforma en sinfonía por influencia de la epigenética». Solo depende de ti que te conviertas en el director de orquesta de esa sinfonía al adoptar un modo de vida sano.
No nos cansaremos de repetirlo: los mecanismos epigenéticos están influidos por nuestros hábitos de vida y por el medio ambiente en el que vivimos. La suerte no está definitivamente echada. Aunque tengas más de cincuenta años, todavía te es posible alterar el curso de las cosas realizando varios esfuerzos. A este respecto, la farmacopea no tardará en acudir en nuestra ayuda. Diversos estudios con ratas han demostrado, en efecto, que interviniendo en los mecanismos epigenéticos con la ayuda de inhibidores o activadores químicos específicos es posible prolongar la supervivencia de los animales y retrasar el deterioro de su memoria cuando envejecen.
Las células madre, ¿portadoras de inmortalidad?
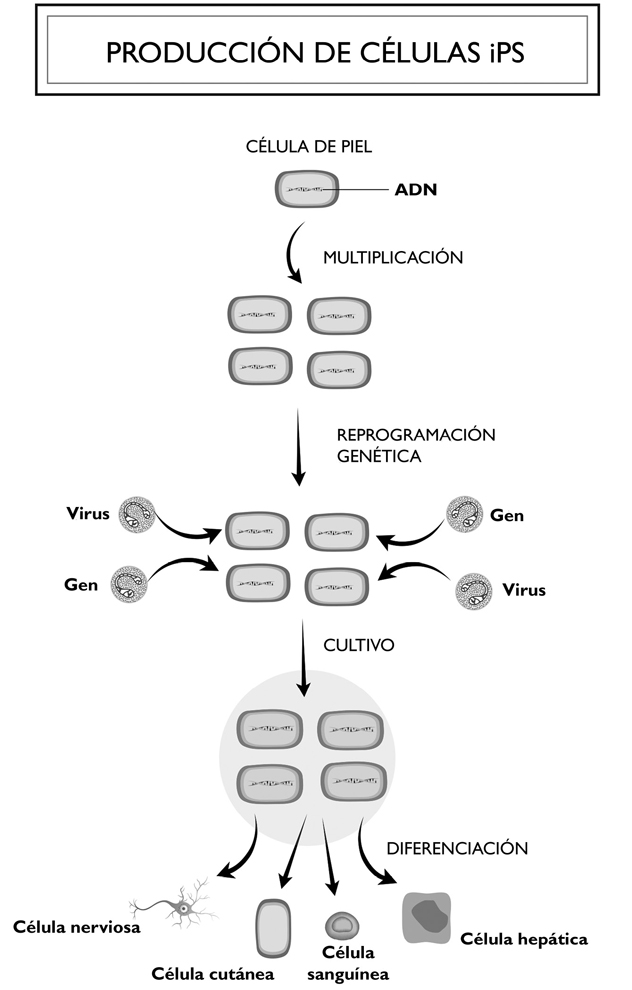
Casi todas las células que componen nuestro cuerpo son altamente especializadas. Una célula cardíaca no se parece a una célula ósea ni a una cutánea. Sin embargo, todas derivan de células madre comunes, presentes en el embrión. Estas células madre embrionarias (CME) son células no diferenciadas que todavía no se han especializado. Las CME son pluripotentes, es decir, que conservan el potencial de generar cualquier tipo de célula por división celular. Pasado el estadio embrionario, cuando una célula madre se divide, una de las dos células hijas permanece idéntica a la célula madre, mientras que la otra se diferencia según las necesidades del organismo. Lamentablemente, el potencial de autorregeneración de las células madre disminuye con el paso de los años, lo que durante mucho tiempo llevó a creer que dichas células desaparecían con la edad. No fue sino hasta los años noventa cuando los científicos pudieron poner en evidencia la persistencia de células madre en los tejidos adultos del ser humano. Reencontramos las células madre adultas (CMA) en pequeñas cantidades en numerosos tejidos, donde sirven de centinelas para reparar los daños que puedan sobrevenir. Su potencial de regeneración es, no obstante, restringido. Por lo general, solo pueden diferenciarse en células pertenecientes al tejido donde residen. Por ejemplo, una célula madre sanguínea puede producir glóbulos blancos, glóbulos rojos o plaquetas, pero no células óseas ni células neuronales. Ahora bien, el japonés Shinya Yamanaka descubrió en 2006 que algunas células adultas bien diferenciadas, como las de la piel, podían ser «reprogramadas» introduciendo en ellas un cóctel de tres o cuatro factores específicos, con el fin de incitarlas a volver a convertirse en células madre. Dicho descubrimiento supone una verdadera revolución, que le valió el premio Nobel de Medicina en 2012. Estas células reprogramadas se denominan iPS (induced pluripotent stem cells, células madre pluripotentes inducidas). Poseen las mismas características que las células madre embrionarias. Se las puede multiplicar fácilmente en cualquier tipo celular y no provocan fenómenos de rechazo cuando se las utiliza en terapia.
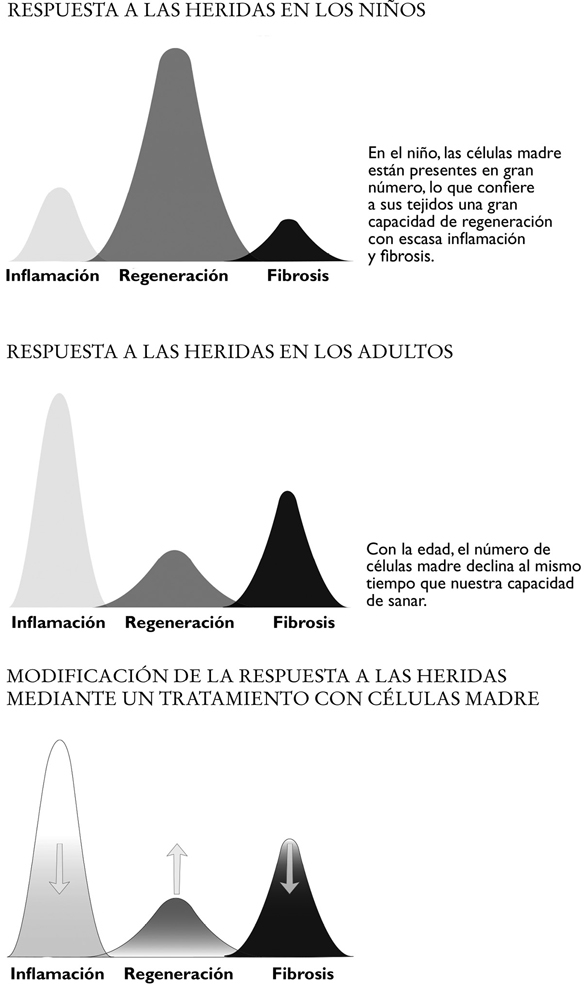
Las aplicaciones potenciales de las células madre inducen a soñar, sobre todo, en medicina regenerativa y antiedad. En un futuro próximo, el dominio de esta tecnología debería permitir regenerar tejidos y órganos que se creían dañados de manera irreversible. Actualmente en todo el mundo se hallan en curso numerosos estudios clínicos que utilizan células madre. Las aplicaciones son diversas: reparación del cartílago (heridas deportivas, artritis, osteoartritis), regeneración de los tejidos oculares (degeneración macular, glaucoma), enfermedades del sistema nervioso (Parkinson, Alzheimer, esclerosis lateral amiotrófica, esclerosis múltiple, parálisis cerebral, lesión de la médula espinal, distrofia muscular), problemas cardíacos (insuficiencia cardíaca, infarto de miocardio, accidente cerebrovascular), enfermedades metabólicas (diabetes de tipo 2), dolencias intestinales (enfermedad de Crohn), cánceres (leucemias, linfomas, tumores sólidos), regeneración de la piel (úlceras, grandes quemados). Varias de estas patologías van ligadas a la edad, de modo que un tratamiento con células madre podría devolver al cuerpo envejecido su capacidad de regeneración.
La microbiota intestinal, modulador de longevidad
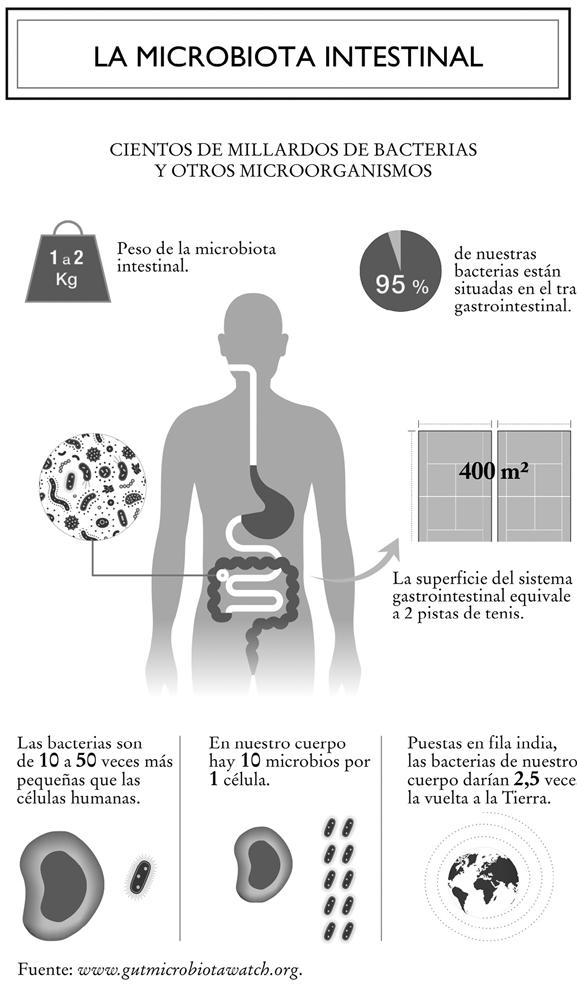
«Microbiota intestinal» es una nueva denominación para designar la flora intestinal, es decir, el conjunto de los microorganismos que colonizan nuestro intestino. ¡Y vaya si es una colonia numerosa! Por sorprendente que parezca, el intestino contiene más de 100.000 millardos de bacterias, virus y hongos. En nuestro cuerpo, los microbios son, de hecho, diez veces más numerosos que las células. Son mucho más pequeños que estas, pero de todos modos darían 2,5 veces la vuelta a la Tierra si los pusiéramos en fila india. Estos microorganismos tapizan el conjunto de los cuatrocientos metros cuadrados de superficie del tracto gastrointestinal, es decir, ¡el equivalente a dos pistas de tenis! En conjunto, la microbiota intestinal puede pesar hasta dos kilos, ¡lo que supera el peso del cerebro, que es aproximadamente de un kilo y medio!

La microbiota toma forma desde los primeros instantes de vida. En el caso de un niño nacido por vía natural y alimentado al pecho, son ante todo las bacterias de la madre las que colonizarán su intestino. A continuación, durante los primeros años de vida, la microbiota se diversificará con la introducción de nuevos alimentos. La microbiota de un adulto en buen estado de salud puede comprender hasta mil especies distintas, la mayoría beneficiosas, por lo general con dos familias dominantes, los firmicutes y los bacteroidetes. La composición de la microbiota varía de un individuo a otro, pero en general permanece estable en un mismo individuo durante su vida adulta. No obstante, la enfermedad, así como un cambio de dieta o de medio ambiente, pueden modificar ese equilibrio. Algunos estudios recientes realizados en diversos países han informado asimismo de cambios importantes ligados al envejecimiento. Así, ciertas bacterias beneficiosas se hallan menos presentes en las personas mayores, mientras que otras, no tan favorables para nuestra salud, adquieren progresivamente importancia. Se constata también una reducción de la diversidad de la microbiota intestinal con la edad. Estos cambios cuantitativos y cualitativos se producen paralelamente al debilitamiento del sistema inmunitario y al desarrollo de un estado inflamatorio crónico de baja intensidad que acompaña a diversas patologías asociadas al envejecimiento.
En comparación con la microbiota intestinal de un adulto sano: reducción de los firmicutes y las bifidobacterias. Aumento de los bacteroidetes y las proteobacterias.
Los microorganismos que colonizan nuestro intestino no son huéspedes pasivos. Influyen directamente en el funcionamiento del organismo a través de diversos mecanismos que veremos más detalladamente en el capítulo siguiente, dedicado a la nutrición. Estos microorganismos modulan el estado de salud y la longevidad. En efecto, los desequilibrios en la composición de la microbiota se han asociado con diversas patologías, como las enfermedades inflamatorias intestinales, el cáncer colorrectal, la obesidad, las alergias, el autismo, y también con patologías crónicas más específicamente ligadas a la edad, como el síndrome metabólico, la diabetes de tipo 2 y las enfermedades neurodegenerativas. Sin embargo, no estamos por completo a merced de nuestra microbiota. Por fortuna, es posible intervenir para proteger o restablecer el equilibrio de los microorganismos que la componen. Puede hacerse llevando una vida activa y favoreciendo una alimentación sana y equilibrada, que cabe mejorar mediante la ingestión de probióticos y prebióticos, como veremos en el capítulo siguiente. En casos extremos de desajuste de la microbiota intestinal, podemos recurrir al trasplante de microbiota fecal. Se trata de transferir las bacterias fecales de un donante sano a un receptor con dificultades. Puede que la técnica no sea elegante, pero posee tremenda eficacia a la hora de tratar las infecciones por Clostridium difficile, con una tasa de curación de más del 90 %. En la actualidad se hallan en curso en todo el mundo pruebas clínicas focalizadas en otras patologías vinculadas a la microbiota (como la obesidad, los trastornos metabólicos, el Parkinson y el Alzheimer). ¿Y si finalmente la microbiota se convirtiera en nuestra aliada de cara a una longevidad incrementada?
¿QUIÉN PUEDE ESPERAR LLEGAR A VIEJO?
Como veremos a lo largo de este libro, los factores que pueden influir en la esperanza de vida son numerosos. En primer lugar, veamos lo que nos enseñan las estadísticas.
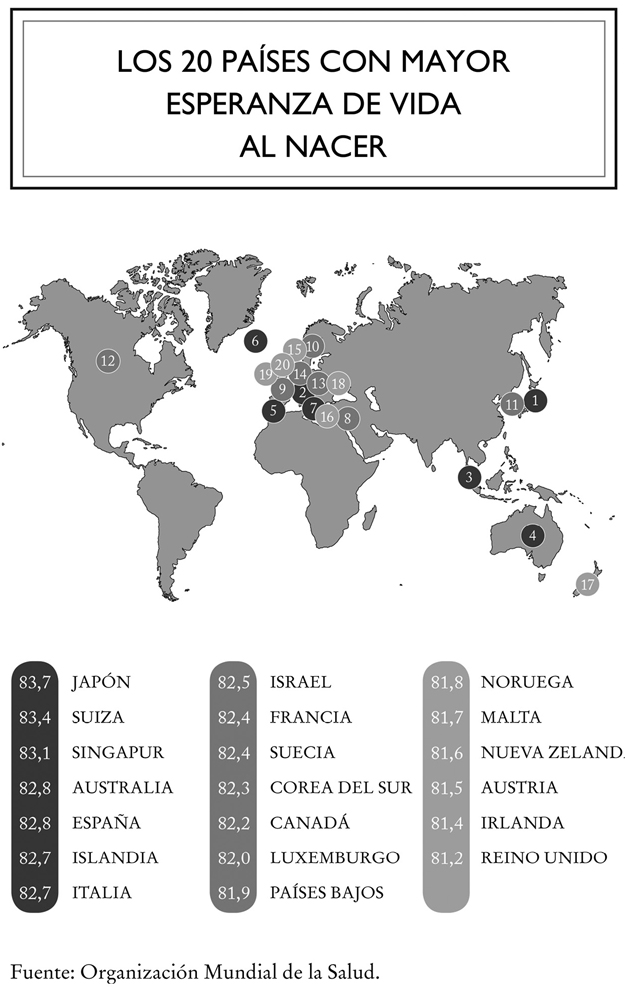
La esperanza de vida ha mejorado de manera espectacular desde el año 2000. Según la Organización Mundial de la Salud (OMS), hemos ganado globalmente cinco años entre 2000 y 2015. A escala mundial, hoy una niña nacida en 2015 puede confiar en vivir 73,8 años, y un niño 69,1 años. Huelga decir que existen grandes disparidades según los países y las regiones. Para los 29 países de renta más elevada, la esperanza media de vida es de 80 años como mínimo, mientras que para los 22 países más pobres es inferior a 60 años. Canadá, Quebec y Francia salen bien librados. En 2015 la esperanza de vida al nacer (sin distinción de sexos) se estimaba en 82,2 años en Canadá (12º puesto mundial), mientras que Quebec la superaba, con 82,4 años, al igual que Francia, también con 82,4 años (9º puesto mundial). Japón venía en primer lugar, con una esperanza de vida de 83,7 años. En lo más bajo de la escala, los países del África subsahariana mostraban globalmente una esperanza de vida limitada a 59 años.
Según todos los indicios, la prolongación de la esperanza de vida no va a detenerse. Un artículo publicado en febrero de 2017 en la muy respetada revista médica The Lancet informa de proyecciones más bien optimistas para 2030. Basándose en modelos matemáticos, los autores de esa investigación predicen que la esperanza de vida al nacer alcanzará ese año 90,8 años para las niñas surcoreanas y 84,1 años para los niños del mismo país. Corea del Sur superará entonces a Japón como campeona del mundo de la longevidad. Siempre según dicha investigación, las niñas francesas se calificarán en el 2º puesto (88,6 años) y los niños franceses en el 17º puesto (81,7 años). Las niñas canadienses obtendrán el 10º puesto (87,1 años) y los niños canadienses el 4º puesto (83,9 años). Estos datos concuerdan sensiblemente con los de Statistique Canada, que predice una esperanza de vida para los que nazcan en 2030 de 86,6 años en el caso de las canadienses y de 82,6 años en el de los canadienses. En cuanto a Quebec, las proyecciones son de 86,4 años para las niñas y de 82,0 años para los niños. El aumento de la esperanza de vida en dichas regiones se atribuye principalmente al acceso universal a cuidados sanitarios de calidad así como a una buena higiene de vida.
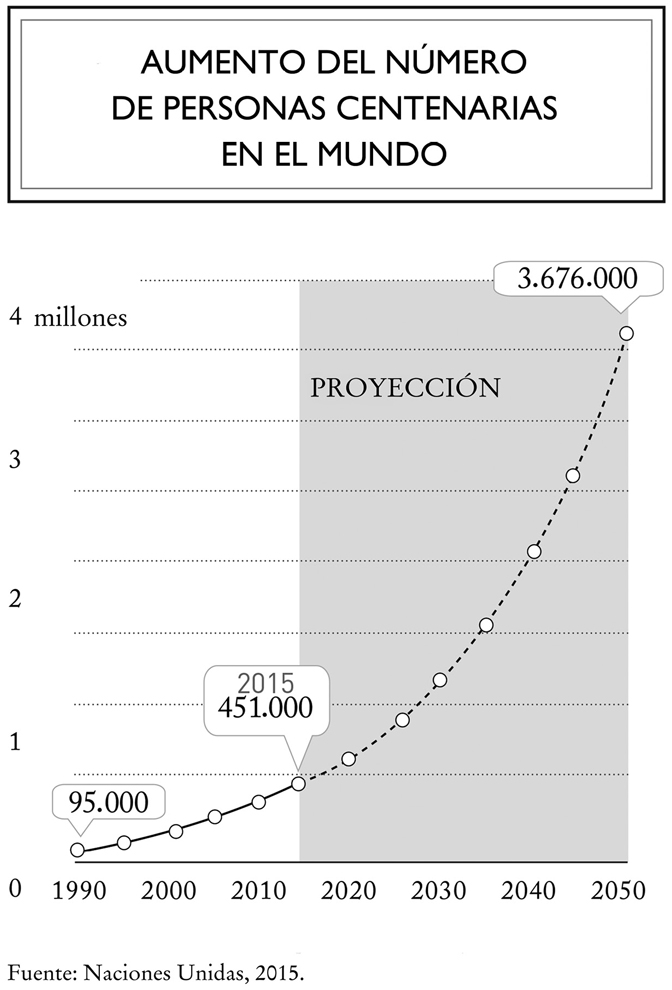
Como consecuencia del aumento de la esperanza de vida, el número de centenarios se incrementa con rapidez en todo el mundo. De 95.000 individuos en 1990, dicha población pasó a 451.000 en 2015. La tendencia incluso debería acelerarse en el curso de los próximos años. Según las proyecciones de Naciones Unidas, en 2050 habrá unos 3,7 millones de centenarios en la Tierra, un aumento de más del 700 % con respecto a 2015. Así, de 1990 a 2050 la proporción de centenarios en el seno del grupo de los mayores de 65 años casi se habrá decuplicado. No obstante, si bien cada vez más personas llegan a centenarias, la duración de vida máxima progresa poco. El récord de longevidad sigue desde 1997 en poder de la francesa Jeanne Calment, fallecida ese año a la edad de 122 años. Se requerirán avances científicos y médicos importantes para confiar en prolongar la vida más allá de los 125 años.
¿DÓNDE RESIDE EL PLACER DE EXISTIR EN TODO ELLO?
Así pues, deberíamos prepararnos para vivir cada vez más años. Ahora bien, ¿podremos contar con la calidad de vida? ¿Envejeceremos con salud? A ese respecto, la OMS nos informa de que, sin distinción de países, una persona nacida en 2015 puede confiar en vivir 64,6 años en buen estado de salud si es una niña y 61,5 años si es un niño. Lo cual significa que al final de su vida nuestros pequeños ciudadanos de todo el mundo deberán transigir con cierta forma de incapacidad durante 9,2 años (mujer) y 7,6 años (hombre). Según los datos de Statistique Canada, en Quebec, en 2006, las mujeres podían contar con vivir con un problema de salud durante sus 14,7 últimos años de vida, y los hombres durante 11,8 años. En Francia, según los datos de Eurostat de 2014, se habla más bien de 21,8 años con un problema de salud para las mujeres y de 16,1 años para los hombres. Primera constatación: de manera general, las mujeres viven más años que los hombres, pero pasan más tiempo con mala salud. Segunda constatación: parece ser que la prolongación de la duración de la vida no siempre se lleva a cabo en las mejores condiciones. Así, según los datos de Eurostat, para los franceses el porcentaje de años vividos en buen estado de salud en relación con la esperanza de vida incluso ha disminuido entre 2006 y 2014, pasando del 76,2 % al 74,7 % en las mujeres y del 81,3 % al 79,7 % en los hombres.
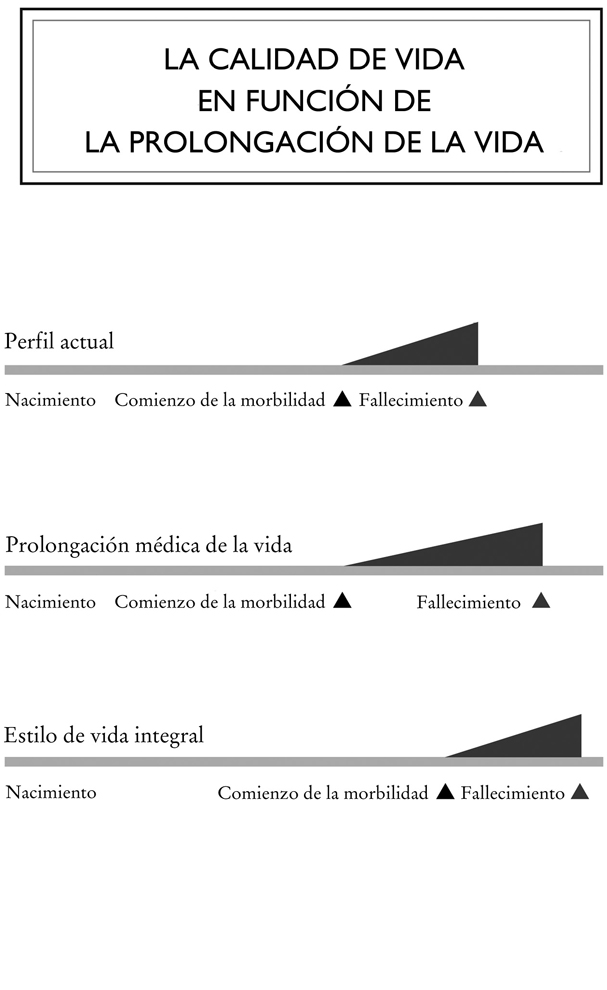
Cabe esperar que los avances científicos y médicos presentes y futuros sigan prolongando nuestra esperanza de vida. Sin embargo, habría que evitar que ello se tradujera en una morbilidad más acusada, es decir, en un mayor número de personas enfermas durante más tiempo al final de su vida. No basta con sumar años a la existencia, también hay que preservar la calidad de la misma. Eso es precisamente lo que te proponemos hacer al adoptar el modelo de vida integral descrito en este libro. Cada capítulo pretende aportar una clave adicional para permitirte llegar a centenario con buena salud y feliz.
¿Eres del tipo jugador, mecánico o jardinero?
No siempre somos conscientes de la percepción que tenemos de nuestro propio cuerpo. No obstante, los prejuicios que albergamos a su respecto condicionan nuestra actitud ante la vida e influyen en gran medida en el modo en que envejecemos. Hagamos un breve alto para tratar de identificar a qué tipo de individuo correspondemos mejor.
El tipo jugador: para él, como para el 20 % de la gente, la vida es una cuestión de azar y se juega con una tirada de dados. Suele ser fumador, tener sobrepeso y vivir la vida a tope. Si le recomiendas que preste más atención a su salud, te hablará del amigo muerto a los 40 años de cáncer de pulmón sin haber fumado jamás. Su frase fetiche: «De algo hay que morir...»
El tipo mecánico: al igual que el 50 % de la gente, considera su cuerpo como un mecanismo que la tecnología médica reparará en caso de avería. Si le diagnostican un problema de salud modificable, como la diabetes de tipo 2, optará por la medicación en vez de cambiar su estilo de vida. Su frase fetiche: «El cuerpo es un hermoso mecanismo que se desgasta irreversiblemente con el tiempo...»
El tipo jardinero: como el 30 % de la gente, sobre todo mujeres, cree que la salud se cultiva día a día. Permanece atento a las señales de su cuerpo y no vacila en modificar sus hábitos cuando es necesario. Se mantiene activo de cuerpo y mente y se siente responsable de su bienestar. Su frase fetiche: «Envejecer es un privilegio que hay que merecer...»
Esperamos de todo corazón que la lectura de este libro te proporcione los medios para devenir y seguir siendo el jardinero de una vida larga y dichosa.
GUÍA PRÁCTICA
Ahora te proponemos realizar un breve test en internet (en inglés) que tiene por objeto evaluar tu esperanza de vida actual. Se trata de un cuestionario al que te recomendamos responder de la forma más sincera posible. Es un test divertido y que debería ayudarte a identificar los hábitos de vida que tendrías que cambiar para vivir feliz, sentirte joven y permanecer en buen estado de salud.
El test de longevidad de Harvard (tal es su nombre) fue desarrollado por los médicos e investigadores Thomas Perls y Margery Hutter Silver. El cuestionario se basa en las observaciones que se derivan de un amplio estudio referido a los centenarios de Nueva Inglaterra, Estados Unidos, realizado a finales de los años noventa.
He aquí el enlace para acceder al test de longevidad de Harvard:
clarityhealthcare.net/longevity_calc.html#aboutcalc
(página consultada el 11-03-2017).
Con el fin de ayudarte a cumplimentar este test en línea, aquí tienes la traducción:
Responde a todas las preguntas y luego clica el botón «Calculate» al pie de la página para descubrir tu esperanza de vida, calculada en función de tus respuestas. La columna «Score» sirve para cifrar automáticamente tus respuestas.
1. ¿Eres fumador, o no fumador rodeado de fumadores?
2. ¿Cueces el pescado, las aves de corral y la carne hasta que están muy hechos?
3. ¿Evitas comer mantequilla, bollería, fritos (por ejemplo, patatas fritas) y grasas saturadas?
4. ¿Comes poca carne y prefieres la fruta, la verdura y la fibra?
5. ¿Bebes más de dos copas de cerveza, vino o licor al día?
6. ¿Bebes cerveza, vino o licor moderadamente, es decir, menos de dos copas al día?
7. ¿Hay advertencias de contaminación atmosférica donde vives?
8. ¿Tomas más de medio litro de café al día?
9. ¿Bebes té a diario?
10. ¿Te tomas una aspirina todos los días?
11. ¿Utilizas seda dental diariamente?
12. ¿Por lo general te pasas más de dos días sin evacuar?
13. ¿Has sufrido alguna crisis cardíaca o accidente cardiovascular?
14. ¿Te gusta broncearte?
15. ¿Tienes un sobrepeso de más de 10 kilos?
16. ¿Vives cerca de tu familia (dejando aparte a tu cónyuge y tus hijos) y pasas con frecuencia a verlos de improviso?
17. a) El estrés me consume, no consigo librarme de él.
b) Consigo librarme del estrés, ya sea rezando, meditando, practicando ejercicio, cultivando el buen humor a diario o por cualquier otro medio.
18. ¿Tus padres murieron por causas naturales antes de cumplir 75 años o necesitaron asistencia diaria al llegar a esa edad?
19. ¿Dos o más de tus parientes, tíos o abuelos, vivieron hasta los 90 años por lo menos?
20. ¿Eres sedentario, es decir, no te mueves de tu casa ni tienes la menor resistencia física?
21. ¿Realizas actividad física al menos tres veces por semana?
22. ¿Tomas vitamina E (400 a 800 unidades internacionales) y selenio (100 a 200 mcg)?
23. ¿Eres hombre o mujer?
CONCLUSIÓN
• El envejecimiento es un fenómeno natural, no una enfermedad ni una maldición.
• Todavía no entendemos muy bien por qué envejecemos, pero diversas teorías nos ofrecen un principio de explicación sobre los mecanismos que pueden ser responsables de ello.
• Los conocimientos científicos y médicos evolucionan con rapidez y constantemente nos proporcionan nuevos medios para frenar el envejecimiento.
• Con la mejora de los cuidados sanitarios y su mayor accesibilidad, la esperanza de vida al nacer ha avanzado de manera prodigiosa estos últimos años, pero la esperanza de vida gozando de buena salud no sigue el mismo ritmo.
• Para vivir más tiempo con salud y felicidad, hay que ser proactivo y adoptar un modelo de vida integral.